Sisällysluettelo
Johdanto
FINGOG-työryhmän laajasta taustamateriaalista kokoama gynekologisten syöpien Kelpo hoito -ohjeisto valmistui ensi kerran joulukuussa 2012. Kyseessä ei ole Käypä hoito -suosituksen tasoinen näyttöön perustuva katsaus, vaan työryhmän käsitys siitä, kuinka gynekologisia syöpiä tulisi hoitaa.
Ohjeiston ensimmäinen päivitys valmistui joulukuussa 2014. Hoito-ohjeisto on kokonaisuudessaan päivitetty helmikuussa 2024. Jatkossa ohjeiston päivitystarpeita tarkastellaan pienryhmässä puolivuosittain, ja niitä tehdään syöpäkohtaisesti aina tarpeen vaatiessa. Päivityksen ajankohta löytyy kunkin syöpätyypin otsikon alta, ja päivitetyt kohdat korostetaan punaisella.
Toivomme ohjeiston palvelevan tarkoitustaan ja helpottavan gynekologisia syöpäpotilaita hoitavien lääkäreiden kliinistä työtä. On huomioitava, että gynekologisten syöpien potilaskohtainen hoito suunnitellaan yhteistyössä yliopistosairaaloiden moniammatillisten hoitokokousten kanssa (MDT). Mikäli potilaan yksilöllisten seikkojen takia poiketaan hoitolinjoista, on se suositeltavaa dokumentoida sairauskertomukseen.
Yhteenveto päivityksistä
Taulukossa luetellaan eri osioiden päivitysten viimeisimmät ajankohdat ja kuvataan tärkeimmät muutokset.
| Osio | Viimeisin päivitys | Kuvaus tärkeimmistä muutoksista |
|---|---|---|
| Ulkosynnytinsyöpä | 16.2.2025 |
|
| Vulvovaginaalinen melanooma | helmikuu 2024 | |
| Emätinsyöpä | helmikuu 2024 | |
| Kohdunkaulasyöpä | 2.6.2025 |
|
| Kohdunrunkosyöpä |
3.10.2025 18.1.2026 |
|
| Kohtusarkoomat | 26.2.2025 |
|
| Epiteliaalinen munanjohdin-, munasarja- ja vatsakalvonsyöpä ja rajalaatuiset kasvaimet |
30.3.2025
24.7.2025 |
|
| Ei-epiteliaalinen munasarjasyöpä | helmikuu 2024 | |
| Trofoblastitaudit | 18.9.2025 |
|
| Perinnöllinen syöpäalttius | 30.3.2025
18.9.2025 |
|
| Gynekologisten syöpien seuranta | 18.1.2026 |
|
| Elämänlaatu – muistilista | 30.3.2025 |
|
Ulkosynnytinsyöpä (levyepiteelikarsinooma)
Päivitetty 16.2.2025.
Suositellut diagnoosikoodit:
C51.01& Ison häpyhuulen levyepiteelikarsinooma
C51.11& Pienen häpyhuulen levyepiteelikarsinooma
C51.21& Häpykielen (klitoriksen) levyepiteelikarsinooma
C51.81& Eri alueisiin ulottuva ulkosynnyttimien levyepiteelikarsinooma
Preoperatiiviset tutkimukset
- Muutosten biopsointi stanssilla tai inkiisiolla, ei ekskiisiolla
- multifokaalisessa taudissa kaikkien leesioiden biopsointi
- P16 määritys kaikista vulvanäytteistä HPV assosiaation määrittämiseksi
- HPV-independent muutoksista p53 IHC
- Kliininen dokumentaatio
- muutoksen sijainti, koko, etäisyys keskiviivaan, etäisyys uretraan, vaginaan ja anukseen, muutoksen mobiliteetti.
- Muutoksen valokuvaaminen mahdollisuuksien mukaan
- HPV-testi cervixistä
- Kuvantaminen:
- Vulvaan tai perineumiin rajautuvia ≤2 cm kasvaimia, joiden invaasiosyvyys ≤1mm, (pT1a tai Ia) ei tarvitse välttämättä kuvantaa
- Nivusten ultraäänitutkimus ja tarvittaessa UÄ-ohjattu biopsia, jos primaarituumori >2cm tai invaasiosyvyys > 1mm (Stage IB)
- jos uä:ssä tulee epäily imusolmukemetastaasista, sitten vartalon TT
- Jos kliinisesti epäily leviämisestä ympäröiviin kudoksiin (urethra, rakko, vagina, anus), suositellaan MRI-tutkimusta kattaen nivuset ja vulva (stage ≥ II)
- Mahdollisen etämetastaasin biopsiaa suositellaan
- Clinical frailility assessment
- Kasvainmerkkiaineena voi käyttää SCC
- HIV harkiten, etenkin nuorilta potilailta
- Suositellaan käyttämään FIGO ja TNM luokitusta rinnakkain
Levinneisyysluokitus
Ulkosynnytinsyövän FIGO-levinneisyysluokitus
| Stage I | Kasvain on rajoittunut ulkosynnyttimiin |
| IA | Kasvaimen koko ≤ 2 cm ja stroomainvaasio ≤ 1 mm |
| IB | Kasvaimen koko > 2 cm tai stroomainvaasio > 1 mm |
| Stage II | Kasvain (koosta riippumatta) ulottuu alimpaan 1/3 uretraan, vaginaan tai anukseen, ei imusolmukelevinneisyyttä |
| Stage III | Kasvain (koosta riippumatta) ulottuu viereisten perineaalisten rakenteiden ylimpiin osiin tai fiksoitumattomia ja ulseroitumattomia imusolmuke-etäpesäkkeitä lukumäärästä riippumatta |
| IIIA | Kasvain (koosta riippumatta) ulottuu ylimpään 2/3 uretraan, tai vaginaan, virtsarakon tai peräsuolen limakalvolle tai paikallisia* imusolmuke-etäpesäkkeitä kooltaan ≤ 5 mm |
| IIIB | Paikallisia* imusolmuke-etäpesäkkeitä kooltaan > 5 mm |
| IIIC | Paikallisia* imusolmuke-etäpesäkkeitä, joissa läpikasvua kapselista |
| Stage IV | Kasvain (koosta riippumatta) fiksoitunut luuhun tai fiksoituneita, ulseroituneita imusolmuke-etäpesäkkeitä, tai kaukometastaasit |
| IVA | Kasvain fiksoitunut luuhun tai fiksoituneita, ulseroituneita imusolmuke-etäpesäkkeitä |
| IVB | Kaukometastaasit |
*) inguinaaliset tai femoraaliset imusolmukkeet
Ulkosynnytinsyövän TNM-levinneisyysluokitus
| T = Primaarikasvain | |
| Tx | Primaarituumoria ei voi arvioida |
| T0 | Ei merkkejä primaarituumorista |
| T1a | Leesio ≤ 2 cm, rajoittuu vulvan tai perineumin alueelle. Stromainvaasio ≤ 1 mm |
| T1b | Leesio > 2 cm tai stroomainvaasio > 1 mm. Rajoittuu vulvan tai perineumin aueelle |
| T2 | Tuumori (koosta riippumatta) ulottuu viereisiin rakenteisiin: uretran tai vaginan distaaliseen kolmannekseen tai peräaukkoon |
| T3 | Tuumori (koosta riippumatta) ulottuu uretran tai vaginan proksimaaliseen 2/3 osaan, virtsarakon limakalvolle, rectumin limakalvolle tai fiksoitunut lantion luisiin rakenteisiin |
| N = Paikalliset imusolmukkeet (inguinaaliset tai femoraaliset imusolmukkeet) | |
| NX | Paikallisia imusolmukkeita ei voi arvioida |
| N0 | Ei imusolmukemetastaaseja |
| N1 | 1-2 paikallista imusolmukemetastaasia: |
| N1a | 1-2 imusolmukemetastaasia, joista kaikki < 5 mm |
| N1b | 1 imusolmukemetastaasi ≥ 5 mm |
| N2 | Paikallisia imusolmukemetastaaseja: |
| N2a | ≥ 3 imusolmukemetastaasia, joista kaikki < 5 mm |
| N2b | ≥ 2 imusolmukemetastaasia ≥ 5 mm |
| N3 | Fiksoituneet tai ulseroituneet imusolmukemetastaasit |
| M = kaukometastaasit | |
| M0 | Ei kaukometastaaseja |
| M1 | Kaukometastaaseja, mukaan lukien lantion imusolmukemetastaasit |
Hoito
Ensileikkaus
- Radikaali paikallispoisto, tavoitteena tuumorivapaat marginaalit
- Jos invasiivinen muutos ulottuu marginaaliin, suositellaan uusinta resektiota
- Distaalisen uretran resektio ≤ 1.5 cm ei yleensä vaikuta pidätyskykyyn
- SLN, jos < 4cm kasvain, > 1 mm invaasio, ei imusolmukemetastaasi epäilyä. Jos muutos ≤1 cm keskiviivasta, bilateraalinen SLN
- jos SLN ei löydy, tulee tehdä nivussolmukkeiden poisto kyseiselle puolelle
- jos SLN todetaan metastaasi, tulee harkita lisätoimenpiteenä joko nivussolmukkeiden poistoa tai sädehoitoa
- jos SLN:ssä makrometastaasi (>2mm), suositellaan kyseisen puolen nivussolmukkeiden poistoa
- jos SLN:ssä mikrometastaasi (≤2mm) tai ICT, annetaan ensisijaisesti sädehoito tai toissijaisesti voi harkita nivussolmukkeiden poistoa
- Jos on tehty bilateraalinen SLN ja todetaan unilateraalinen metastasointi, kontralateraalisen metastaasin riski on matala ja jatkohoito voidaan rajoittaa affisioituneelle puolelle
- ≥ 3 cm tuumoreissa kuitenkin muistettava kontralateraalisen metastasoinnin mahdollisuus
- IF LND, jos > 4cm kasvain tai multifokaalinen muutos
- keskiviivan tuumoreissa bilateraalinen IF LND
- jos metastasointi ipsilateraalisissa imusolmukkeissa, suositellaan myös kontralateraalisten imusolmukkeiden poistoa
- Vartijaimusolmukkeen jääleiketutkimukseen liittyy riski, että mahdollinen mikrometastaasi jää löytymättä lopullisessa leikkeessä tai metastaasin koko ei vastaa todellista kokoa
- Jääleiketutkimus tehdään, jos epäily kliinisesti metastasoinnista vartijaimusolmukkeessa
Kemosädehoito (sädehoito) liitännäishoitona
Liitännäishoitona pääsääntöisesti sisplatiinitehosteisena leikkauksen jälkeen:
- nivusten ja lantion (iliaca interna, iliaca externa ja obturatoriuskuoppa) Annos 45–50.4 Gy 25–28 fraktiossa (1.8-2 Gy /fraktio).
- Vartijaimusolmukkeen ≤ 2 mm metastaasin ja ITC:n ensisijaisena hoitovaihtoehtona on sädehoito (50 Gy) IF LND:n sijaan jos sädehoito päästään aloittamaan alle 6 viikkoa leikkauksesta
- Mikäli vartijaimusolmukkeen metastaasi on > 2 mm, tulee tehdä IF LND ja sen jälkeen kemosädehoito (50 Gy) mikäli todetaan lisää imusolmukemetastaaseja tai ekstrakapsulaarista tuumorin leviämistä
- Mikäli makrometastaaseja tai ekstrakapsulaarista leviämistä, suositellaan IF alueelle boosteria 54-56 Gy (jos makroskooppista tautia ei enää nähtävillä)
- Mikäli makrometastaaseja on vielä jäljellä, annos 64-66 Gy
- Mikäli lantion alueella suurentuneita imusolmukkeita, suositellaan 57-60 Gy boosteria
- vulvaan, jos leikkausmarginaalissa on syöpää eikä lisäresektioon ole mahdollisuutta. Suositellaan 60-66 Gy boosteria ulkoisella sädehoidolla tai brakyterapiaa
- Jos vulvan leikkausmarginaalit (niukat tai) positiiviset, CTV:n tulisi kattaa alue noin 2 cm marginaaleilla. Merkkilankaa voidaan käyttää arvessa booster-alueen määrittämiseksi.
- Vulvan sädehoitoa voidaan harkita, jos useampia paikallisen uusiutuman riskitekijöitä: niukat leikkausmarginaalit (alle 2-3mm), lymfovaskulaarinen tai perineuraalinen invaasio, >5 mm invaasiosyvyys sekä kasvaimen suuri koko
- Marginaalien ollessa negatiiviset, CTV:n tulisi kattaa koko operatiivinen alue. Mikäli vulvassa tai jalassa ödeemaa, voidaan tarvita adaptiivista sädehoitoa tai pehmytkudosten kuvantamisohjausta.
- Hoidon tulisi alkaa niin pian kuin mahdollista ja hoitotaukoja tulisi välttää
- Tavoiteaika alle 15 viikkoa kirurgiasta sädehoidon päättymiseen
- Akuutit haitat (mm. ripuli, uupumus, iho-limakalvoreaktiot) ovat yleisiä ja niiden aktiivinen hoito on tärkeää, jotta hoitotauot tai hoidon keskeyttäminen voidaan välttää
Marginaalit
- Re-resektio vain jos syöpää marginaaleissa
- LS/dVIN/HSIL marginaalissa hoidettava yksilöllisen suunnitelman mukaan ja seurattava pitkään, sillä näillä esiastemuutoksilla marginaalissa on suurempi vaikutus paikallisiin uusitumiin kuin lyhyillä marginaaleilla itsessään
Neoadjuvanttihoito paikallisesti levinneessä taudissa
- Jos kirurginen hoito ensilinjassa vaatii rakko- ja/tai suoliavanteen, voidaan harkita neoadjuvanttihoitoa levinneessä taudissa ja leikkausharkinta tehdään hoitovasteen perusteella
- Työryhmä suosittelee ensisijaisesti neoadjuvanttihoitona platinapohjaista sytostaattihoitoa
- tällöin 3-4 hoitosyklin jälkeen arvio definitiivisestä hoidosta
- Vaihtoehtona kemosädehoito inoperaabelin taudin hoidon mukaisesti
Inoperaabelin taudin hoito
- Definitiivisenä hoitona inoperaabeleille potilaille kemosädehoito ensisijaisesti sisplatiinipohjaisena vulvan ja paikallisten imusolmukkeiden alueelle sekä booster vulvan alueelle brakyterapialla tai ulkoisella sädehoidolla.
- Hoitoalue: koko vulva, lantion imusolmukealueet (yläraja 1 cm iliaca communis- bifurkaation yläpuolella, sisältäen iliaca interna, iliaca externa, obturatorius kuoppa, nivunen syvän femoraaliarterian haaroihin asti), annos min. 50 Gy
- hoitoalueen ylärajaa voidaan tarvittaessa nosta 2 cm kraniaalisimman positiivisen lantion imusolmukkeen yläpuolelle
- PET-positiivisille imusolmukkeille SIB booster ad 60(-66) Gy
- Brakyhoito (interstitielli) yhden viikon aikana vulvan tuumorin alueelle 12-25 Gy, edeltävästi parin viikon tauko EBRT ja BT välillä.
- Jos käytetään externia boosteria vulvaan, voidaan hoitaa annokseen 70 Gy
- Arvioidaan hoitovaste 3 kk kemosädehoidon päättymisestä ja jos tautiresiduaalia, voidaan harkita leikkaushoitoa
- Hoitoalue: koko vulva, lantion imusolmukealueet (yläraja 1 cm iliaca communis- bifurkaation yläpuolella, sisältäen iliaca interna, iliaca externa, obturatorius kuoppa, nivunen syvän femoraaliarterian haaroihin asti), annos min. 50 Gy
- Lantion ulkopuolisiin metastaaseihin voi harkita sädehoitoa paikalliskontrollin saavuttamiseksi
Systeemihoito levinneessä tai uusiutuneessa taudissa
- Harkitse MMR-, PD-L1-, TMB- ja NTRK fuusiogeeni -tutkimuksia
- Levinneen tai uusiutuneen taudin systeemisen hoidon suositeltavin vaihtoehto on sisplatiini/karboplatiini + paklitakseli +/- bevasitsumabi
- Muita vaihtoehtoja ovat sisplatiini, karboplatiini, paklitakseli, sisplatiini+vinorelbiini tai sisplatiini+gemsitabiini
- Kohdunkaulansyöpätutkimuksien perusteella pembrolitsumabia yhdistettynä platinapohjaiseen kemoterapiaan (+/- bevasitsumabiin) voi harkita potilaskohtaisesti (PD-L1 positiivisille [CPS≥1] tai dMMR/TMB-H) edenneessä/uusiutuneessa vulvakarsinoomassa, vaikka lääkettä ei ole virallisesti hyväksytty vulvakarsinooman hoitoon (sairaalakohtainen lupa)
- Mikäli progressio ensilinjan platinapohjaisen hoidon jälkeen, ei ole suositusta standardihoidosta
- larotrektinibi NTRK+ kasvaimissa
Uusiutuneen taudin muut hoidot
Vulvan uusiutumat
- osa uusiutumista uusia primaarikasvaimia, jonka vuoksi kirurgista nivusimusolmukkeiden levinneisyyden selvittämistä tulisi harkita, mikäli ei kliinisesti viitettä IFN metastaasista
- Jos ei aiempaa kirurgiaa nivusten alueille, SLN voidaan harkita
- mikäli mahdollista, radikaali paikallispoisto 2 cm marginaalein tarvittaessa plastiikkakirurgisten kielekkeiden kanssa. Jos imusolmukepoistoja ei ole tehty aiemmin tai on poistettu vain SLN, IF LND kuten aiemmin kuvattu.
- Postoperatiivisen kemosädehoidon indikaatiot noudattavat ensilinjan hoidon indikaatioita
- Laajoissa uusiutumissa voidaan harkita lantion eksenteraatiota
Nivusen uusiutumat
- Laaja kuvantaminen MRI:lla, vartalon TT ja/tai PET-TT tutkimuksella
- Biopsia mahdollisuuksien mukaan
- IF LND tai kirurginen debulking jos mahdollista, ja nivusen kemosädehoito, jos aiemmin ei ole annettu sädehoitoa.
- Muutoin etenemistä jarruttava sytostaattihoito ja muu oireenmukainen hoito.
- Pelkän sytostaattihoidon haitat saattavat ylittää odotettavissa olevan hyödyn
Lantion alueen imusolmukeuusiutumat
- suositellaan kemosädehoitoa jota edeltävästi voi harkita kirurgista debulkingia
Kaukouusiutumat
- Jos yksittäinen kaukouusiutuma, kirurgiaa tai stereotaktista sädehoitoa voidaan harkita biopsiavarmennuksen jälkeen
- muussa tilanteessa systeemihoidot
Palliatiivinen hoito
- varhainen palliatiivinen hoito parantaa oireiden kanssa pärjäämistä ja loppuelämän hoitoa
- palliatiivista kirurgiaa voidaan harkita tietyissä tilanteissa
- kontinenssin menetyksen / virtsaummen hoito (avanteet, rakkokatetrit/-diversiot)
- kroonisten haavojen hoito
- kivun hoito (lääkitys, paikallispuudutteet, kipusädehoito)
Muu hoito
- alaraajaturvotuksen ehkäisy ja hoito: lääkinnälliset hoitosukat, lymfaterapia, painemansettihoito, liikunta, painonpudotus, iho-ongelmien ennaltaehkäisy ja tehokas varhainen hoito
- introituksen ja vaginan ahtautuminen: venytyshoidot, limakalvojen paikallishoidot, paikalliset kirurgiset plastiat introitukseen
- seksuaalista ja psykososiaalista neuvontaa tulee tarjota
- paikallisestrogeeni
- sädehoidon aiheuttamassa varhaisessa menopaussissa hormonikorvaushoitoa tulee harkita
- urologin tai gastroenterologin konsultaatio, jos sädehoidosta pitkäaikaisia elämänlaatua heikentäviä virtsarakko- tai suolihaittoja
Kirjallisuusviitteet
Vulvovaginaalinen melanooma
Päivitetty helmikuussa 2024.
Suositellut diagnoosikoodit:
C51.03& Ison häpyhuulen melanooma
C51.13& Pienen häpyhuulen melanooma
C51.23& Häpykielen (klitoriksen) melanooma
C51.83& Eri alueisiin ulottuva ulkosynnyttimien melanooma
Preoperatiiviset tutkimukset
- Vulva ja vagina tutkitaan aina gynekologisessa asennossa
- Poikkeavat alueet kuvaillaan huolellisesti potilaskertomukseen (tarkka sijainti kellotaululla, laatu, määrä, koko, etäisyys keskilinjaan ja kriittisiin rakenteisiin)
- Valokuvat muutoksesta
- Biopsiat stanssilla (≥ 4mm), ei veneviiltoa, vältetään ekskiisiota
- Biopsoidaan kaikki pigmentoituneet muutokset
- Maligneja melanoomia 5-10% vulvan maligniteeteista
- Nodular, superficial spreading, lentiginous
- Iho vs. limakalvo
- Vulvan melanoomissa erilainen mutaatioprofiili kuin ihomelanoomissa
- BRAF-mutaatiot↓ (3% vs 50%)
- Instabiliteetti ↓
- C-Kit mutaatiot ↑ (imatinibi, nilotinibi)
- Jos palpaation tai melanooman paksuuden (Breslow’n mitta yli 4 mm) perusteella epäillään lähi-imusolmukealueen etäpesäkkeitä, potilaalle tehdään ennen leikkausta imusolmukealueen kuvantaminen (UÄ tai CT) ja epäilyttävistä imusolmukkeista otetaan kuvantamisohjattu neulanäyte (mielellään paksuneulabiopsia)
- Alavatsan MRI vaginan geelitäytöllä voi auttaa leikkauksen suunnittelussa
- Vartalon TT / PET-TT
Levinneisyysluokitus
| T = Primaarikasvain | |
| Tx | Primaarituumoria ei voi arvioida |
| T0 | Ei merkkejä primaarituumorista |
| Tis | Melanoma in situ |
| T1 | Paksuus ≤1.0 mm, ei tietoa ulseraatiosta |
| T1a | Paksuus <0.8 mm, ei ulseraatiota |
| T1b | Paksuus <0.8 mm ja ulseraatio TAI paksuus 0.8-1.0 mm +/- ulseraatio |
| T2 | Paksuus >1.0-2.0 mm, ei tietoa ulseraatiosta |
| T2a | Ei merkkejä primaarituumorista |
| T2b | Ei merkkejä primaarituumorista |
| T3 | Paksuus >2.0-4.0 mm, ei tietoa ulseraatiosta |
| T3a | Paksuus >2.0-4.0 mm, ei ulseraatiota |
| T3b | Paksuus >2.0-4.0 mm ja ulseraatio |
| T4 | Paksuus >4.0 mm, ei tietoa ulseraatiosta |
| T4a | Paksuus >4.0 mm, ei ulseraatiota |
| T4b | Paksuus >4.0 ja ulseraatio |
| N = Paikalliset imusolmukkeet | |
| NX | Paikallisia imusolmukkeita ei voi arvioida |
| N0 | Ei imusolmukemetastaaseja |
| N1 | 1 imusolmukemetastaasi TAI in-transit, sateliitti +/- mikrosatelliitti metastasointi ilman imusolmukemetastaasia |
| N1a | 1 kliinisesti okkultti metastaasi (eli todettu vartijaimusolmuketutkimuksessa) |
| N1b | 1 kliinisesti todettu metastaasi |
| N1c | In-transit, sateliitti +/- mikrosatelliitti metastasointi ilman imusolmukemetastasointia |
| N2 | 2-3 imusolmukemetastaasia TAI in-transit, sateliitti +/- mikrosatelliitti metastasointi sekä yksi imusolmukemetastaasi |
| N2a | 2 tai 3 kliinisesti okkulttia metastaasia |
| N2b | 2-3 imusolmukemetastaasia, joista ainakin yksi on kliinisesti todettu |
| N2c | 1 kliinisesti okkultti tai kliinisesti todettu imusolmukemetastaasi JA in-transit, sateliitti +/- mikrosatelliitti metastasointi |
| N3 | ≥4 imusolmukemetastaasia TAI in-transit, sateliitti +/- mikrosatelliitti metastasointi sekä vähintään kaksi imusolmukemetastaasia TAI yhteenkasvaneet imusolmukemetastaasit |
| N3a | ≥4 kliinisesti okkulttia metastaasia |
| N3b | ≥4 imusolmukemetastaasia, joista ainakin yksi on kliinisesti todettu TAI yhteenkasvaneet imusolmukemetastaasit |
| N3c | ≥2 kliinisesti todettua tai okkulttia metastaasia JA/TAI yhteenkasvaneet imusolmukemetastaasit JA in-transit, sateliitti +/- mikrosatelliitti metastasointi |
| M = Kaukometastaasit | |
| M0 | Ei kaukometastaaseja |
| M1 | Kaukometastaaseja, mukaan lukien lantion imusolmukemetastaasit |
| M1a | Kaukometastasointi iholle, pehmytkudokseen (sis. lihakseen) ja/tai ei-paikallisiin imusolmukkeisiin (ei tietoa LDH tasosta) |
| M1a(0) | Kaukometastasointi iholle, pehmytkudokseen (sis. lihakseen) ja/tai ei-paikallisiin imusolmukkeisiin JA LDH ei ole koholla |
| M1a(1) | Kaukometastasointi iholle, pehmytkudokseen (sis. lihakseen) ja/tai ei-paikallisiin imusolmukkeisiin JA LDH on koholla |
| M1b | Kaukometastasointi keuhkoon +/- M1a levinneisyyden lisäksi (ei tietoa LDH tasosta) |
| M1b(0) | Kaukometastasointi keuhkoon +/- M1a levinneisyyden lisäksi JA LDH ei ole koholla |
| M1b(1) | Kaukometastasointi keuhkoon +/- M1a levinneisyyden lisäksi JA LDH on koholla |
| M1c | Kaukometastasointi sisäelimiin (ei keskushermosto) +/- M1a tai M1b levinneisyys(ei tietoa LDH tasosta) |
| M1c(0) | Kaukometastasointi sisäelimiin (ei keskushermosto) +/- M1a tai M1b levinneisyys lisäksi JA LDH matala |
| M1c(1) | Kaukometastasointi sisäelimiin (ei keskushermosto) +/- M1a tai M1b levinneisyys lisäksi JA LDH koholla |
| M1d | Kaukometastasointi keskushermostoon +/- M1a, M1b tai M1c levinneisyys (e tietoa LDH tasosta) |
| M1d(0) | Kaukometastasointi keskushermostoon +/- M1a, M1b tai M1c levinneisyys JA LDH matala |
| M1d(1) | Kaukometastasointi keskushermostoon +/- M1a, M1b tai M1c levinneisyys JA LDH koholla |

Hoito
Ensileikkaus (vulva)
- Kirurginen marginaali
- Breslow ≤ 2.0 mm: leikkausmarginaali 1 cm
- Breslow > 2.0 mm: leikkausmarginaali 2 cm
- Leikkausmarginaalia suurennetaan, jos primaarituumoriin liittyy satelliittipesäkkeitä
- Radikaali (= alla olevaan faskiaan saakka ulottuva) paikallispoisto tai hemivulvektomia
- preparaattiin voidaan ottaa mukaan ad 1,5 cm uretraa ilman pidätyskyvyn ongelmia
- mukaan myös melanoma in situ
- (pinnallisempi poisto ja) marginaali 5 mm
- Imusolmukkeet
- SLNB suositellaan jos
- Breslow > 1.0 mm ja melanooma on kliinisesti paikallinen (T2-4N0M0)
- SLNB voidaan harkita
- ohuissa T1-melanoomissa (paksuus ≤ 1mm) jos Breslow 0.8-1mm tai melanooma on ulseroitunut, erityisesti jos potilas nuori (<40-50v), primaarikasvaimessa mitooseja tai LVI
- histologisesti vaikeasti tulkittavissa kasvaimissa tai jos melanooman paksuus on jäänyt epäselväksi epäadekvaatin biopsiatavan vuoksi
- SLNB vasta-aiheet
- heikko yleistila, lyhyt elinaikaennusta korkean iän tai vakavien liitännäissairauksien vuoksi
- kliinisesti todetut imusolmuke etäpesäkkeet tai melanooma levinnyt muihin elimiin
- raskausaikana siniväriä (sikiötoksinen)/ICG:ta ei tule käyttää, mutta raskaus ei ole gammakuvaukselle ehdoton vasta-aihe
- Iliakaaliset ja pelviset vartijaimusolmukkeet voidaan jättää poistamatta, jos radioaktiivisimmat vartijaimusolmukkeet pinnallisella nivusalueella
- Vartijaa ei lähetetä jääleikkeeksi
- Jos vartijassa todetaan mikrometastaasi, IF LND ei paranna ennustetta, joten hoidetaan seurannalla/adjuvanttihoidolla
- Jos vartijaa ei löydy, ei näyttöä LND:n ennustetta parantavasta hyödystä
- työryhmä ei suosittele LND:ta, mutta suosittelee nivusten ultraääniseurantaa keskikorkean riskin seurannan mukaisesti
- Täydentävää imusolmukepoistoa puoltavat:
- Metastaattisia vartijaimusolmukkeita ≥ 3
- Metastaasin koko ≥ 4 mm
- Metastaasin invaasio imusolmukkeen ulkopuolelle rasvakudokseen
- Primaarituumorin satelliittipesäkkeet
- Vartijasolmukkeen imutieinvaasio
- Potilaan immunosupressiivinen lääkitys
- Mahdollisesti myös jos Breslow ≥ 4.0 mm ja/tai melanooman ulseraatio
- SLNB suositellaan jos
- IF LND uni-/bilateraalisesti
- Jos kliinisesti nivusmetastaasi (palp/rtg + PAD)
Ensileikkaus (vagina)
Vaginan melanooman kirurginen hoito (laaja ekskiisio, lantion eksenteraatio, APR) suunnitellaan yksilöllisesti
Adjuvanttihoito
- Adjuvanttihoidosta konsultoidaan onkologia
- Sädehoito parantaa paikalliskontrollia, ei elinaikaa
- Tulisi harkita potilaalle, jolla suuri riski paikallisresidiiville (suuri residuaalitaudin määrä, läpikasvu kapselista, makroskooppinen imusolmukemetastaasi, ≥3 nivusimusolmukemetastaasia tai yksittäinen metastaasi ≥ 4 cm)
- Voidaan harkita, jos niukat tai positiiviset marginaalit eikä re-resektion mahdollisuutta, jos aloitus alle 6 vkoa kirurgiasta (paitsi jos systeemistä hoitoa annetaan ennen sädehoitoa)
Levinneen taudin hoito
- Konsultoidaan onkologia
- IO-hoidoilla vasteet vähäisempiä limakalvo- kuin ihomelanoomissa
- Sytostaattien teho vähäinen
- Palliatiivinen sädehoito tarvittaessa.
Uusiutuneen taudin hoito
- Paikallisuusiutuma arvessa
- radikaali paikallispoisto 1-2 cm tervekudosmarginaaleilla ± rekonstruktiivinen kirurgia
- imusolmukekartoitusta ei tehdä uudelleen rutiinisti mikäli se on tehty jo primaarihoitovaiheessa
- Satelliitti- tai in-transit uusiutuma
- operoitavissa
- radikaali paikallispoisto puhtain marginaalein
- systeeminen adjuvanttihoito
- ei operoitavissa
- systeeminen hoito
- Paikallinen uusiutuma imusolmukkeessa
- operoitavissa
- metastaasin poisto ja täydentävä LND, jos ei aiemmin ole tehty
- systeemisen adjuvanttihoidon harkinta
- ei operoitavissa
- systeeminen hoito
- palliatiivinen sädehoito, jos aiemmin ei ole annettu
- muu oireenmukainen hoito
- Kaukouusiutuma
- hoito riippuu metastaasien määrästä ja paikasta
- resektio, stereotaktinen sädehoito, systeeminen hoito, palliatiivinen sädehoito
- muu oireenmukainen hoito
Kirjallisuusviitteet
Emätinsyöpä
Päivitetty helmikuussa 2024.
Levinneisyystutkimukset
- Kolposkopia, biopsiat
- levinneisyystutkimukset: vartalon TT/PET-TT, sekä alavatsan tai lantion MRI
Tuumorin koko ja lokalisaatio (ylin, keski- tai alin kolmannes) pitää tarkentaa ja dokumentoida, samoin HPV-assosiaatio. Stagingissa tulisi käyttää FIGO-stagingin rinnalla myös TNM-luokitusta.
- emättimen yläkolmanneksen kasvaimen hoito noudattaa kohdunkaulasyövän hoitolinjoja, alakolmanneksen kasvaimen hoito ulkosynnytinsyövän hoitolinjoja
- imunestekierto vaginan yläosasta lantion imusolmukkeisiin, alaosasta nivustaipeiden imusolmukkeisiin ja keskikolmanneksesta molempiin imusolmukealueisiin

Hoito
Ensivaiheen hoito (levyepiteelikarsinooma)
STAGE 1
- Kirurginen hoito
- Radikaalin leikkauksen ja sädehoidon yhdistelmää vältettävä komplikaatioitten ja sivuvaikutusten vuoksi
- Kirurgiaa voidaan harkita vain alle 2 cm tuumoreissa, jotka eivät ole anuksen tai uretran lähellä, jotta saadaan puhtaat marginaalit ilman urologisia/G-i- kirurgisia toimenpiteitä
- pyritään 1 cm marginaaleihin (marginaalit oltava puhtaat, ei tunnettuja minimimarginaaleja)
- Vartijaimusolmuketutkimuksesta ei ole vielä tarpeeksi näyttöä emätinsyövässä
- Emättimen yläosan kasvain (2 ylintä kolmannesta)
- radikaali kohdunpoisto + emättimen yläosan poisto + iliakaalinen LND
- Emättimen alakolmanneksen kasvain
- paikallinen poisto ja nivusimusolmukkeiden LND
- leikkauksen jälkeen (kemo-)sädehoito, jos kasvain ulottuu poistoreunoihin tai imusolmukemetastasointi
- Kemosädehoitoa suositellaan imusolmukepositiivisissa, mutta voi myös harkita marginaalipositiivisissa
- Radikaalin leikkauksen ja sädehoidon yhdistelmää vältettävä komplikaatioitten ja sivuvaikutusten vuoksi
- Sädehoito
- Definitiivinen kemosädehoito (sisplatiini herkistäjänä) leikkauksen sijaan usein ensisijainen varsinkin yli 2 cm ja vaginan keski- tai alaosan tuumoreissa
- pieni pinnallinen tuumori max. 2cm kooltaan ja alle 7 mm paksuudeltaan, voidaan harkita hoidettavan pelkällä brakysädehoidolla imusolmukestagingin jälkeen
- Yleensä lantion ulkoinen kemosädehoito + brakyhoito
- noudatetaan pääosin cervixca:n sädehoitoa
- tuumorin alueelle kokonaistavoiteannos 70-80 Gy
- lantion ja/tai nivusten imusolmukealueille 45-50 Gy
- ovarioitten transpositiota voi harkita premenopausaalisilla
- kokonaishoitoaika kemosh + braky ei saa ylittää 7-8 vkoa
- pieni pinnallinen tuumori max. 2cm kooltaan ja alle 7 mm paksuudeltaan, voidaan harkita hoidettavan pelkällä brakysädehoidolla imusolmukestagingin jälkeen
- Definitiivinen kemosädehoito (sisplatiini herkistäjänä) leikkauksen sijaan usein ensisijainen varsinkin yli 2 cm ja vaginan keski- tai alaosan tuumoreissa
STAGET II, III ja STAGE IVa
- yleensä hoidetaan sädehoidolla, kts. alempaa
- yksittäisissä tapauksissa lantion eksenteraatioleikkaus voi tulla kyseeseen (kookas fisteli jo primaaristi tai sädehoito kontraindisoitu), mutta tutkimusnäyttö on vähäinen. Harkittava neovaginan mahdollisuus.
- neoadjuvanttihoidosta ei näyttöä
STAGE IVb
- oligometastaattisessa primääritaudissa definitiivinen kemosädehoito + braky + sytostaattihoito (joissain tapauksissa resektio tai stereotaktinen sädehoito)
- hyväkuntoiselle potilaalle laajalle levinneessä taudissa platinapohjainen sytostaattihoito cx-ca:n hoito-ohjetta mukaillen
- palliatiivinen sädehoito
- palliatiivinen hoito, tarv. Stoomat/stentit
- Immunologinen hoito harkittavissa PDL-1- positiivisilla cx-ca:n hoito-ohjetta mukaillen
Definitiivisen kemosädehoidon toteutus
- ulkoinen sädehoito 45 GY lantion ja imusolmukkeiden alueelle annetaan kuten kohdunkaulasyövässä kemosädehoitona (sisplatiini 40 mg/m2 kerran viikossa)
- jos sisplatiini ei käy, karboplatiini tai fluorourasiili
- Jos hoidetaan vaginan alaosan syöpää, myös nivusimusolmukkeet sädehoidetaan
- Tarvittaessa myös para-aortaalialueen imusolmukkeiden hoito, ei profylaktisesti
- Metastaattiset imusolmukkeet voidaan boostata ulkoisen sädehoidon yhteydessä. Kokonaisannos niihin (brakyhoidon vaikutuksen kanssa) tulisi olla 55-60GY.
- Brakyhoidolla pyritään annokseen 75-85GY tuumorin alueella, vaginan alaosa herkempi sädehoidolle (kuin vulva), otettava huomioon annoksen suunnittelussa, jopa 70 GY voi riittää
Uusiutuneen taudin hoito
Paikallinen uusiutuma
- PET-CT suositellaan levinneisyyden selvittämiseen
- jos sädehoitoa ei ole annettu, kemosädehoito/sädehoito (+brakyterapia),
- jos on, onko uudelleen sädetys mahdollista?
- jos paikallinen sentraalinen residiivi, jossa puhtaat marginaalit saavutettavissa, lantion eksenteraatioleikkausta voi harkita
- jos ei aktiivisemmin hoidettavissa: platinapohjainen sytostaattihoito yksinään tai kombinaationa kuten kohdunkaulan syövässä
- Immunologisia hoitoja ei ole vaginakarsinoomassa laajemmin tutkittu taudin harvinaisuuden vuoksi, mutta cx- karsinooman ja vulvakarsinooman hoitoja voi soveltaa (pembrolitsumabi PDL-1 positiivisilla)
Laajemmalti uusiutuneessa samat hoitovaihtoehdot kuin stage IVB- taudissa.
Harvinaiset histologiset tyypit
- adenokarsinooma/kirkassoluinen adenokarsinooma
- harvinainen, hoito samoin kuin levyepiteelisyövässä
- sarkoomat
- kirurginen hoito ensisijainen
Kirjallisuusviitteet
Kohdunkaulasyöpä
Päivitetty 2.6.2025.
Levinneisyystutkimukset
- lantion MRI tuumorin koon ja parametrioinvaasion selvittämiseksi
- voidaan jättää pois, jos T1a tauti loop-konisaatissa puhtain marginaalein
- vartalon TT/vartalon PET-TT
- vartalon PET-TT on suositeltava ainakin stage IB3 lähtien imusolmukelevinneisyyden ja metastasoinnin selvittämiseksi ja mikäli varhaisvaiheen taudissa todetaan kuvantaen epäilyttäviä imusolmukkeita
- levinneisyysluokituksessa käytetään sekä TNM että FIGO 2018 levinneisyysluokitusta
Levinneisyysluokitus FIGO/TNM 2018
| Stage I | IA mikroskooppinen tauti, invaasiosyvyys < 5 mm
IA1 invaasiosyvyys < 3 mm IA2 invaasiosyvyys ≥ 3 mm mutta < 5 mm IB kohdunkaulaan rajoittunut, invaasio ≥ 5 mm IB1 invasiivisen karsinooman invaasiosyvyys ≥5 mm ja suurin mitta alle 2 cm IB2 invasiivinen karsinooma ≥ 2 cm mutta < 4 cm IB3 invasiivinen karsinooma ≥ 4 cm |
| Stage II | IIA levinneisyys kohdun ulkopuolelle mutta ei emättimen alakolmannekseen tai parametrioon
IIA1 kasvaimen suurin mitta <4 cm IIA2 kasvaimen suurin mitta ≥ 4 cm IIB parametriolevinneisyys |
| Stage III | Levinneisyys vaginan alakolmannekseen ja/tai lantion sivuseinämään ja/tai aiheuttaa hydronefroosin tai on levinnyt imusolmukkeisiin
IIIA levinneisyys vaginan alakolmannekseen mutta ei lantion seinämään IIIB levinneisyys lantion sivuseinämään ja/tai aiheuttaa hydronefroosin IIIC imusolmukelevinneisyys IIIC1 vain lantion imusolmukkeisiin IIIC2 para-aortaalisiin imusolmukkeisiin |
| Stage IV | Levinneisyys virtsarakkoon tai rektumiin (limakalvolle) tai kaukaisempiin elimiin
IVA levinneisyys virtsarakkoon tai rektumiin tai lantion ulkopuolelle IVB kaukolevinneisyys kuten metastasointi kaukaisiin imusolmukkeisiin, luustoon, keuhkoihin |
N0 ei imusolmukemetastasointia
N=i+ (isoloidut tuumorisolut < 0.2 mm)
N1 imusolmukemetastasointi
M0 ei kaukometastaaseja
M1 kaukometastaasit (supraklavikulaariset/mediastinumin/ei-regionaaliset imusolmukemetastaasit, peritoneum, maksa, keuhko, luusto)
Histopatologinen arviointi
- arvioidaan WHO 2020 luokituksen mukaisesti
- tuumorin koko tulee määritellä konisaatista/kohtupreparaatista sekä tervekudosmarginaalit
- invaasiosyvyys kohdunkaulaan tulee mitata ja ilmoittaa myös jäljellä oleva tervekudosmarginaali kohdunkaulassa
- gradeeraus ei ole levyepiteelimuutoksissa välttämätöntä, mutta adenokarsinoomissa suositellaan käytettävän Silva-luokitusta
- imutie-, verisuoni- ja perineuraalinen invaasio tulee ilmoittaa
- esiasteleesioiden olemassaolo tulee mainita
- imusolmukkeiden lukumäärä ja status tulee raportoida, samoin vartijasolmukkeiden ja luokiteltava löydökset mikro/makrometastaaseihin
Silva-luokitus ja imusolmukemetastasointiriski: A ei imusolmukemetastasointiriskiä, B < 4 % riski imusolmukemetastasointiin, C n. 20 % riski imusolmukemetastasointiin
Hoito
Stage IA1 LVI negatiivinen (invaasiosyvyys < 3mm)
- konisaatio tai tavallinen kohdunpoisto
- imusolmukemetastasointiriski <1%; ei tarvetta imusolmukkeiden poistolle, residivointiriski <3%
- konisaatin on oltava marginaaleiltaan puhdas (myös preinvasiivisen osalta, paitsi LSIL)
- jos marginaali positiivinen, uusintakonisaatio
Stage IA1 LVI positiivinen (invaasiosyvyys < 3mm)
- konisaatio tai tavallinen kohdunpoisto sekä vartijaimusolmuketutkimus
- imusolmukemetastasointiriski 2-8%, parametriolevinneisyysriski <1%
Stage IA1 adenokarsinooma (invaasiosyvyys < 3mm)
- konisaatiolla hoidetuille suositellaan kohdunpoistoa, kun lapset tehty
Stage IA2 (invaasiosyvyys ≥ 3mm mutta < 5mm)
- konisaatio tai tavallinen kohdunpoisto sekä vartijaimusolmuketutkimus
- (imusolmukemetastasointiriski 2-8%, parametriolevinneisyysriski <1%)
- kohdunpoistoa suositellaan adenokarsinoomissa, kun lapset tehty
Fertiliteetin säästävä hoito Stage IB1 (invasiivisen karsinooman invaasiosyvyys ≥5mm ja suurin mitta alle 2cm)
- Fertiliteetin säästävästä hoidosta aina konsultoitava gyn.onkologia ja hoidonsuunnittelu sekä toimenpide tulee tehdä yliopistollisessa sairaalassa
- Alle 2 cm kokoisissa tuumoreissa voidaan tehdä konisaatio tai yksinkertainen (simple) trakelektomia mikäli potilaalla on raskaustoive- ja mahdollisuus, levyepiteeli tai usual type (HPV taustainen) adenokarsinooma tai adenosquamous karsinooma, stroomainvaasio <10mm, ei imusolmukemetastasointia, puhdas marginaali tulee olla ≥5mm
- fertiliteettiä säästävää hoitoa ei suositella neuroendokriinisissa, HPV-negatiivisissa adenokarsinoomissa eikä karsinosarkoomissa
- simple trakelektomiassa poistetaan kohdunkaula, mutta säilytetään kohdun runko-osa ja emätin sekä munasarjat ja munanjohtimet, tehdään vartijaimusolmuketutkimus
- radikaalin trakelektomian indikaationa on stage IB1 lvsi positiivinen kasvain
- pysyvä Cerclage tulee laittaa trakelektomian yhteydessä
- imusolmukemetastasointi poissulkee fertiliteetin säästävän hoidon
Stage IB1: invasiivisen karsinooman invaasiosyvyys ≥ 5 mm ja suurin mitta alle 2 cm
- tavallinen kohdunpoisto ja SLN tai kemosädehoito + brakyterapia (BT)
- tavallisen kohdunpoiston edellytys on kasvaimen invaasio alle 10 mm kohdunkaulan stroomaan konisaatissa. Lisäksi loopkonisaatin marginaalien on oltava syövästä puhtaat eikä saa olla imutieinvaasiota
- histologia: levyepiteelikarsinooma G1-3, G1-2 usual type adenokarsinooma, tai adenoskvamoosi karsinooma
- mini-invasiivista leikkaustapaa voidaan käyttää matalan riskin taudeissa, kuten kasvaimen koon ollessa ≤ 2 cm ja konisaatin marginaalien ollessa puhtaat. Hoitavalla keskuksella tulee olla kokemusta mini-invasiivisesta kirurgiasta ja ESGO:n laatukriteereiden tulee täyttyä. Potilasta tulee huolellisesti myös informoida.
Stage IB2: invasiivinen karsinooma ≥ 2cm mutta < 4cm, sekä Stage IIA1: karsinooma levinnyt kohdun ulkopuolelle mutta ei emättimen alakolmannekseen tai parametrioon, < 4cm
- radikaali kohdunpoisto (tyyppi B-C, taulukko 1.) ja SLN tai kemosädehoito+ brakyterapia (BT)
- laparotominen leikkaus on suositeltu standardi leikkaustapa
- mini-invasiivista leikkaustapaa voidaan käyttää vain matalan riskin taudeissa, kuten kasvaimen koon ollessa ≤2cm ja konisaatin marginaalien ollessa puhtaat. Hoitavalla keskuksella tulee olla kokemusta mini-invasiivisesta kirurgiasta ja ESGOn laatukriteereiden tulee täyttyä. Potilasta tulee huolellisesti myös informoida.
Stage IB3: invasiivinen karsinooma ≥ 4 cm, sekä Stage IIA2: karsinooma levinnyt kohdun ulkopuolelle mutta ei emättimen alakolmannekseen tai parametrioon, ≥ 4 cm
- ensisijaisesti kemosädehoito + BT
Radikaalin kohdunpoiston tyypin (parametrioresektion laajuuden) määrittävät preoperatiiviset riskitekijät, Kts. Taulukko 1.
Taulukko 1: Preoperatiiviset riskitekijät
| Riski | Tuumorin koko | LVIS | Stroomainvaasio | Radikaalin kohdunpoiston tyyppi (kts. taulukko 2) |
|---|---|---|---|---|
| Matala | <2 cm | Negatiivinen | Sisäkolmannes | B1 (A) |
| Keskitaso | ≥2 cm | Negatiivinen | Mikä tahansa | B2 (C1) |
| <2 cm | Positiivinen | Mikä tahansa | B2 (C1) | |
| Korkea | ≥2 cm | Positiivinen | Mikä tahansa | C1 (C2) |
Taulukko 2. Querleu-Morrow 2017 luokitus radikaalista kohdunpoistosta
| Tyyppi | Lateraalinen parametrio | Ventraalinen parametrio | Dorsaalinen parametrio |
|---|---|---|---|
| A | Kohdunkaulan ja ureterin puolesta välistä | Minimaalisesti | Minimaalisesti |
| B1 | Ureterin tasosta | Osittainen vesikouterina lig. resektio | Osittainen rektouterina-rektovag. lig. ja uterosakraalisen poimun resektio |
| B2 | Kuten B1+parakervik. lymfadenektomia | Kuten B1 | Kuten B1 |
| C1 | Iliaka-suonten tasolta poikittaisesti, kaudaalinen osa säästetään | Vesikouterina ja vesikovag. lig. resektio | Rektumin tasolta (hypogastriset hermot säästetään) |
| C2 | Iliaka suonten tasolta sisältäen kaudaalisen osan | Virtsarakon seinämän tasosta (virtsarakon hermoja ei säästetä) | Sakrumin tasolta (hypogastrisia hermoja ei säästetä) |
- Premenopausaaliselta potilailta ei tarvitse poistaa munasarjoja, jos kyseessä levyepiteelikarsinooma tai usual type (HPV-taustainen) adenokarsinooma
- Jos todetaan mikro (0.2-2 mm) tai makro (> 2 mm) metastasointi lantion imusolmukkeissa jääleikkeessä, lantion lymfadenektomiaa tai radikaalia kohdunpoistoa ei suositella tehtäväksi ja sen sijaan suositellaan kemosädehoitoa + BT:aa. Para-aortaalista lymfadenektomiaa suositetaan vähintään arteria mesenterica inferiorin tasolle taudin levinneisyyden määrittämiseksi.
- Suositus kohdunpoiston välttämisestä intraoperatiivisesti todetussa imusolmukelevinneisyydestä perustuu retrospektiivisiin tutkimuksiin, joiden mukaan ei kuitenkaan todettu eroa onkologisessa ennusteessa tai residivoinnissa eikä sivuvaikutuksissa. Mahdollisesti leikkauksen ja sädehoidon yhdistelmään liittyy enemmän alaraajojen imunestekierron häiriötä, ja pelkkään sädehoitoon enemmän suoli/virtsatieoireita ja seksuaalifunktion toimintahäiriöitä.
- Radikaalia kohdunpoistoa tulee välttää, jos on todennäköistä, että potilas tarvitsisi leikkauksen jälkeen adjuvanttihoitoa. Siinä tapauksessa hoitona on kemosädehoito ja BT.
- Neoadjuvantti solunsalpaajahoidosta ennen kirurgiaa ei ole suositeltavaa
- Mikäli potilas on leikattu riittävällä laajuudella huomioiden hänen preoperatiiviset riskitekijänsä (Taulukko 1.), voidaan siirtyä seurantaan leikkauksen jälkeen, muutoin tulee harkita adjuvanttia sädehoitoa tai kemosädehoitoa
- postoperatiivinen adjuvantti sädehoito parantaa tautivapaata aikaa muttei elossa oloa, mikäli todetaan positiivinen LVSI, kohdunkaulan pinnallinen stroomainvaasio (1/3) ja kasvaimen koko > 5 cm, tai stroomainvaasio keskikolmannekseen ja kasvaimen koko on > 2 cm tai stroomainvaasio ulkokolmannekseen (ns. Sedlis-kriteerit). Histologinen tyyppi tulisi kuitenkin huomioida, sillä levyepiteelisyövissä kohdunkaulan invaasiolla on suurempi merkitys ja adenokarsinoomissa taas kasvaimen koolla.
- korkean riskin tapauksissa (imusolmukemetastasointi tai positiiviset marginaalit tai parametrioinvaasio (korkean riskin tauti), annetaan kemosädehoito postoperatiivisesti
- Harvinaisissa kohdunkaulan syövissä (neuroendokriininen karsinooma, karsinosarkooma, erilaistumaton karsinooma, lymfooma) hoito suunnitellaan yksilöllisesti
Stage IIB-IVA (IIB: parametriolevinneisyys, III: karsinooma levinnyt vaginan alakolmannekseen ja/tai lantion sivuseinämään ja/tai aiheuttaa hydronefroosin tai on levinnyt imusolmukkeisiin, IVA: levinnyt viereisiin elimiin) ja uusiutunut tauti
- Kemosädehoito + BT
- hoitoon liitetään pembrolitsumabi 200 mg (tai flatdose) iv. 3 viikon välein, mikäli kasvain ulottuu emättimen alakolmannekseen, lantion sivuseinämään/hydronefroosi, tai viereisiin elimiin (FIGO Stage III-IVA 2014) , potilaan suorituskyky on ECOG 0-1 ja GFR > 50 eikä estettä immuno-onkologiselle hoidolle ole todettavissa (Keynote-A18)
- sädehoidon päätyttyä pembrolitsumabi 400 mg jatkuu ylläpitohoitona 6 viikon välein 15 sykliä, ellei merkittäviä haittoja tai taudin etenemistä todeta
- Induktiokemoterapiaa tulee tarkkaan harkita ennen kemosädehoitoa (imusolmukkeisiin levinnyt max ad aortabifurkaatio: karboplatiini AUC2 ja paklitakseli 80 mg/m2 viikottain kuuden viikon ajan (Interlace trial) eikä se ole suositeltavaa kuin erityisistä syistä
- Ulkoinen sädehoito yhteensä 45 Gy 1.8 Gy:n fraktiossa 25 kertaa viiden viikon aikana
- Para-aortaalialue otetaan sädehoitokenttään, mikäli iliaca communis alueella on todettu radiologisesti tai histologisesti yksikin etäpesäke imusolmukkeessa. Nivusalueen imusolmukkeet otetaan sädehoitokenttään, mikäli syöpä ulottuu emättimen alakolmannekseen. (Suurentuneiden imusolmukkeiden poistoa ei suositella ennen kemosädehoitoa)
- Inoperaabelin primaarituumorin annos 25 x 1.8 Gy = 45 Gy kohdunkaulan syövän hoidossa
- lisäksi näkyvien imusolmuke-etäpesäkkeiden sädehoito (PET-TT-pohjainen) samanaikaisena SIB-hoitona (= simultanious integrated boost)
- Iliaca externa ja interna sekä obturatorius-alueen imusolmukkeet kertafraktiolla 2.2 Gy (= 25 x 2.2 Gy= 55 Gy)
- iliaca communis/para-aortaaliset/inguinaaliset imusolmukkeet kertafraktiolla 2.3 Gy (= 25 x 2.3 Gy = 57.5 Gy)
- Primaarituumoria ei boostata ulkoisella sädehoidolla
- Kemosädehoidossa sisplatiini 40 mg/m2 x 5-6 kerran viikossa (maksimiannos kerrallaan 70 mg).
- Vaihtoehtona viikottainen karboplatiini AUC 2, niille joille ei sisplatiinia voida antaa.
- Mikäli kohdunkaulansyöpäpotilaalle suunnitellaan kuratiivista lantion alueen ulkoista kemosädehoitoa ja brakysädehoitoa, tulee tieto ulkoisen kemosädehoidon alkamisesta ilmoittaa mahdollisimman varhain brakysädehoitoa antavaan yksikköön BT:n aikataulun ja hoidon suunnittelemiseksi, kemosädehoidon ja BT:n kokonaishoitoaika ei saisi ylittää 7 viikkoa
- BT toteutetaan 3D-kuvantaen, ensisijaisesti MRI: annostavoitteena HR-CTV D90 85-95 Gy
- Mikäli ainoastaan ontelonsisäisellä BT:lla ei saavuteta riittävää kattavuutta kasvainalueelle tai riskielinten annokset ylittävät suositellut rajat (virtsarakko < 80 Gy, rektum < 65 Gy, sigma < 70 Gy, vagina < 65 Gy), kudoksensisäinen BT on paras vaihtoehto
- kudoksensisäisen BT:n indikaatiot (neulahoidot) arvioinnin apuna voi käyttää seuraavia:
- kasvain ulottuu keskiviivasta lateraalisuuntaan 35 mm kohdunkaulan ulkosuun tasolla
- pisteen A tasolla kasvain ulottuu yli 25 mm lateraalisuuntaan
- symmetrinen sädehoitojakauma ulottuisi riskielimeen
- kudoksensisäisen BT:n indikaatiot (neulahoidot) arvioinnin apuna voi käyttää seuraavia:
- definitiivisen kemosädehoidon ja brakyhoidon jälkeen ei suositella kemoterapiaa eikä kohdun poistoa, koska ne eivät paranna taudin ennustetta
- Sädehoidon jälkeen sentraalisesti uusiutuneessa, paikallisesti levinneessä taudissa lantion eksenteraatioleikkausta voidaan harkita
Stage IVB (kaukometastasointi), hoitoresistentti tai uusiutunut tauti
- Suositellaan solunsalpaajahoidon (paklitakseli 135 mg/m2 tai 175mg/m2 pv1+sisplatiini 50mg/m2 pv1, tai paklitakseli +karboplatiini) ja bevasitsumabin (15mg/kg 3 viikon välein) yhdistelmää
- hoito jatkuu, kunnes tauti etenee tai ilmaantuu kohtuutonta toksisuutta tai saavutetaan täydellinen hoitovaste
- PD-L1-positiivisilla hoitoon yhdistetään pembrolitsumabi (ad 35 sykliä)
- PD-L1-negatiivisilla potilailla, joilla tauti etenee platinahoidon jälkeen, hoitona voidaan antaa semiplimabia (Libtayo; EMAN indikaatio) 350 mg iv-infuusio 30 min 3 viikon välein, jos he eivät ole saaneet aiemmin immunologista hoitoa
- uusiutuneessa taudissa suositellaan PD-L1-positiivisille ensisijaisesti pembrolitsumabia, mikäli aiemmin ei ole saanut immuno-onkologista lääkehoitoa
Toisen linjan yksittäisiä sytostaattivaihtoehtoja
| Vaikuttava aine | n | CR+PR, % | PFS (kk) | OS (kk) |
| karboplatiini | 41 | 15 | ||
| bevasitsumabi | 46 | 11 | 3.4 | 7.3 |
| topotekaani | 94 | 13–19 | 2.1–2.4 | 6.4–6.6 |
| vinorelbiini | 44 | 14 | – | – |
| gemsitabiini | 22 | 5 | 2.1 | 6.5 |
| NAB-paklitakseli | 35 | 29 | 5 | 9.4 |
| doketakseli | 23 | 9 | 3.8 | 7 |
| premeteksedi | 72 | 14–15 | 2.5–3.1 | 7.4–8.8 |
| irinotekaani | 42 | 21 | 4.5 | 6.4 |
| PLD | 27 | 11 | 3.2 | 8.9 |
- Uusiutuneessa taudissa hoidon luonne on palliatiivinen ja potilas tulisi ohjata tehokkaaseen palliatiiviseen hoitoon mahdollisimman varhain. Aiemmin todettu mediaani OS on ollut keskimäärin 7 kk.
Kirjallisuusviitteet
Kohdunrunkosyöpä
Päivitetty 18.1.2026.
Kohdunrunkosyöpä on yleisin gynekologinen maligniteetti. Tämä päivitetty hoitosuositus perustuu uusimpaan ESGO-ESTRO-ESP 2025 -suositukseen1 ja FIGO 2023 -levinneisyysluokitteluun2, joka integroi molekyyliluokituksen kliiniseen käyttöön – koko suositus on päivitetty 3.10.2025.
Diagnostiikka ja staging
Kliininen tutkimus ja kuvantaminen
- Diagnostiikka perustuu gynekologiseen tutkimukseen ja kuvantamiseen (emättimen ultraääni ja/tai lantion MRI)
- Kaukometastasoinnin poissulkuun käytetään ensisijaisesti vartalon TT-kuvausta, vaihtoehtoisesti MRI tai PET-TT
- Intraoperatiivista jääleikettä ei suositella huonon toistettavuuden vuoksi
Luokittelu:
- Konventionaalinen luokittelu: kasvaintyyppi, histopatologinen luokitus, stage, lymfovaskulaarinen invaasio (LVI)
- Molekulaarinen luokittelu: p53, MMRd / MSI, POLE-mutaatio
Histologiset alatyypit:
- Atyyppinen hyperplasia: mikäli endometrium on poikkeava, hoidon suunnittelu gyn. onkologisessa yksikössä
- Ei-aggressiivinen:
- Hyvin tai kohtalaisesti erilaistunut adenoca, low grade G1-G2
- Aggressiivinen:
- Huonosti erilaistunut adenoca, high grade G3, seroosi, kirkassoluinen, erilaistumaton, karsinosarkooma, sekamuotoinen, muut kuten mesonefroidi, intestinaalinen musinoosi, neuroendokriininen
Patologianäytteiden käsittely ja molekulaariset tutkimukset
- Kaikista kasvaimista määritetään molekulaarinen luokka: MMR (MLH1, PMS2, MSH2, MSH6) ja p53:n immunohistokemia, POLE-sekvenointi, jos vaikuttaa potilaan liitännäishoitoon (kuvat 1 ja 2)
- ER ja PR määritys kaikille
- Molekyyliluokitus voidaan tehdä endometriumnäytteestä preoperatiivisesti
- p53-mutaatiossa, seroosissa histologiassa ja karsinosarkoomassa tehdään HER2-immunohistokemia

Kuva 2. Kohdunrungon syövän molekulaaristen luokkien selvittäminen Suomessa immunohistokemiallisten tutkimusten (MSI ja p53-mutaatio) ja POLE-sekvenoinnin avulla.
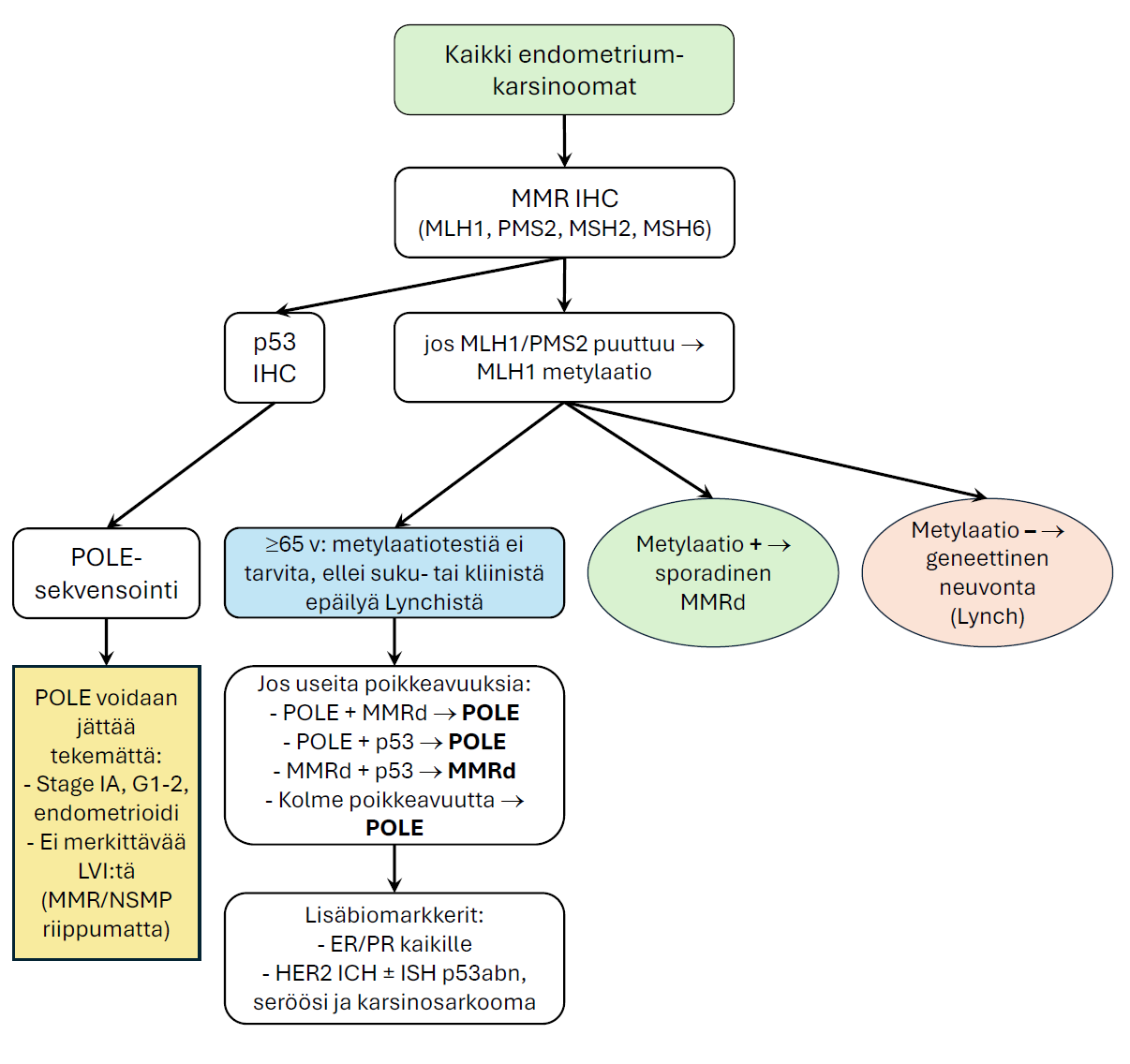
FIGO 2023 -levinneisyysluokitus ja riskiluokat
Käytetään yksityiskohtaisesti uutta FIGO 2023 -luokitusta, jonka mukaisesti tauti jaetaan tarkemmin paikallisen levinneisyyden ja molekulaaristen piirteiden mukaan.
Histologian ja molekulaarisen luokituksen yhdistäminen riskiluokituksessa
Riskiluokat, arvioitu uusiutumariski 5 v seurannassa:
- matala riski < 8%
- keskitason riski 8-15%
- korkea keskitason riski 15-25%
- korkea riski > 25%
- POLE-mutatoitunut: hyvä ennuste
- MMRd ja NSMP: keskikorkea riski
- p53, ER-: huono ennuste (NSMP ER- sama ennuste kuin p53mut)
Riskiluokitus tehdään yhdistämällä FIGO 2023 staging ja molekyyliluokitus (kuvat 3A ja 3B):
- Matala riski: POLE mut, MMRd/NSMP G1-G2 endometroidi, rajoittunut myometriumin ja invaasio < 50%, LVI- tai fokaalinen
- Keskitasoinen riski: MMRd/NSMP ilman merkittävää LVI:ta, G1-G2 syvä inv, G3/nonendometroidi matala inv
- Korkea keskitason riski: MMRd/NSMP, endometroidi, merkittävä LVI tai kohdunkaulan strooman invaasio
- Korkea riski: MMRd/NSMP endometroidi/nonendometroidi, ER-negatiivinen tai p53mut, paikallinen leviäminen, ei jäännöskasvainta
- Levinnyt/metastaattinen: Stage III–IVA jäännöskasvainta tai IVB, mikä tahansa molekylaarinen alatyyppi
Kuva 3A. Integroitu riskiluokitus, kohtuun rajoittunut tauti (1)
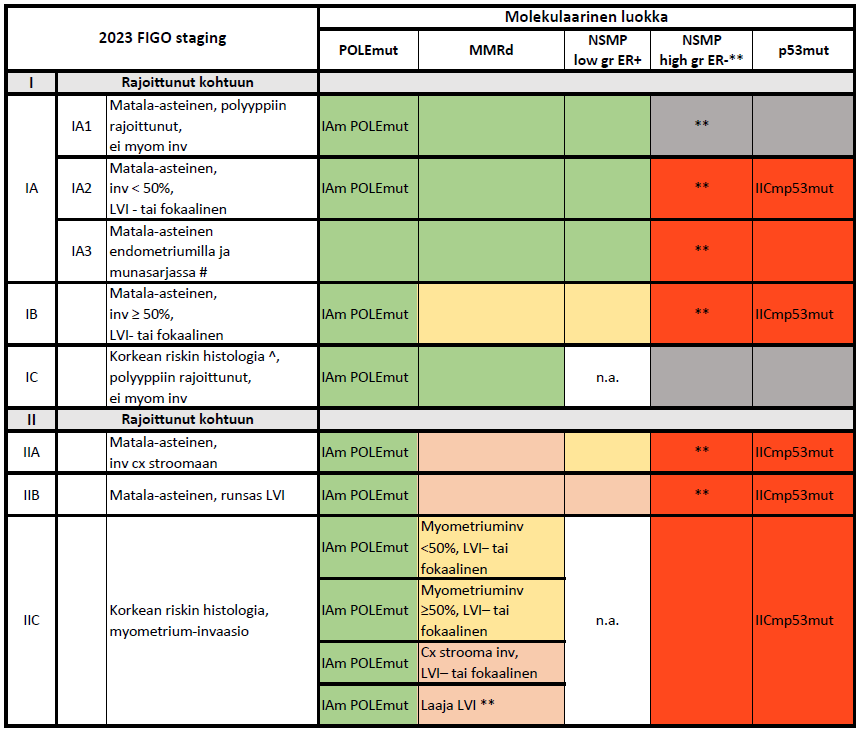
Riskiluokkien värikoodaus:
Vihreä: matala riski
Keltainen: keskitason riski
Vaaleanruskea: korkea keskitason riski
Punainen: korkea riski
Harmaa: epäselvä riski
Kuva 3B. Integroitu riskiluokitys, paikallisesti ja alueellisesti levinneet sekä metastaattiset taudit (1).
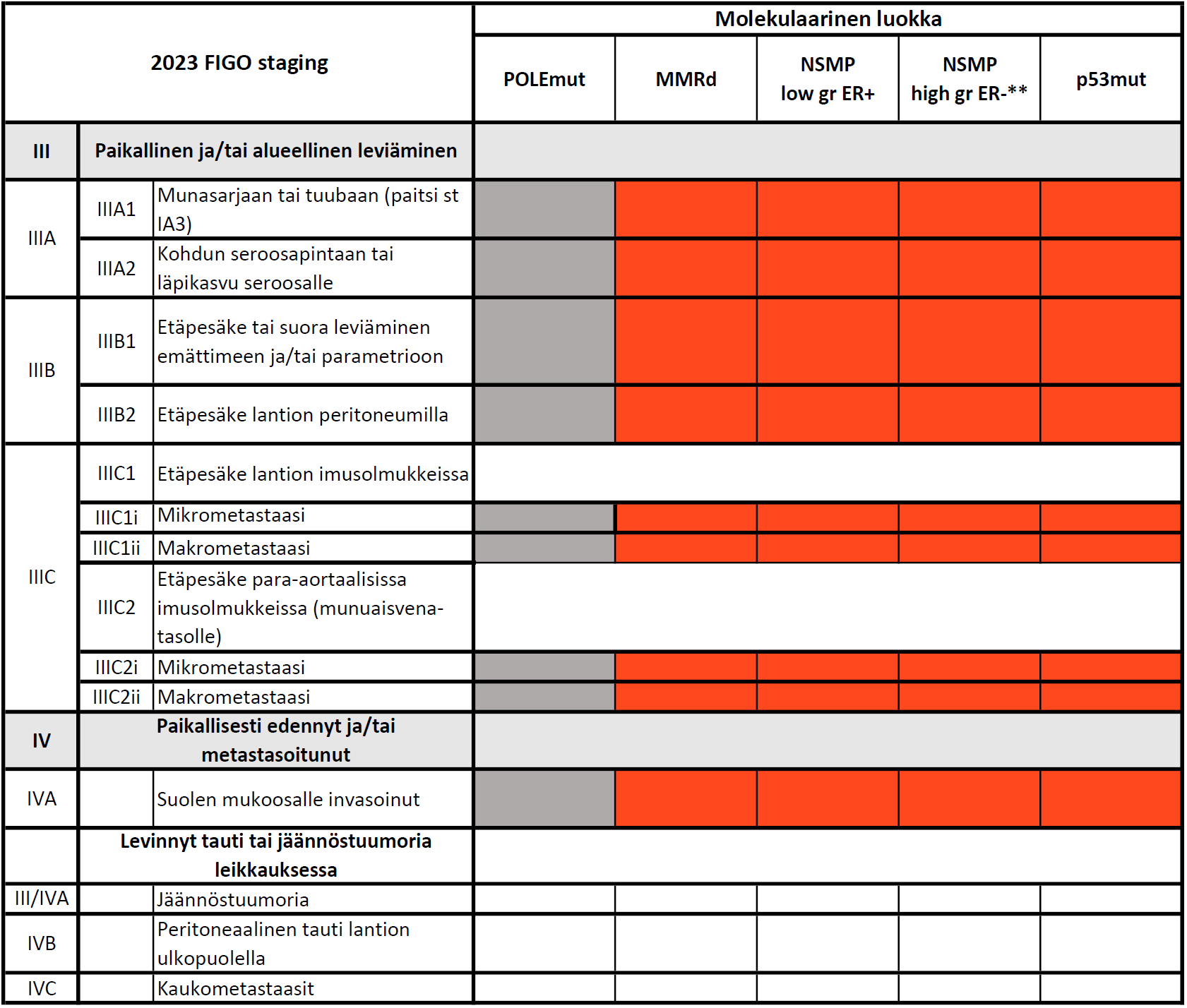
Riskiluokkien värikoodaus:
Punainen: korkea riski
Harmaa: epäselvä riski
Selitykset:
** NSMP high gr ER- sisältää joko huonosti erilaistuneen NSMP:n tai ER-negatiivisen NSMP:n.
# myometriuminvaasio <50% + LVI– tai fokaalinen + munasarjatuumori pT1a
^ G3, seroosi, kirkassoluinen, karsinosarkooma, erilaistumaton, sekatyyppinen, mesonefroidi, musinoottinen gastrointestinaalinen
Hoito
Kirurginen hoito
Standardihoito kohtuun rajoittuneessa syövässä: Minimaalisesti invasiivinen kirurgia; hysterektomia ja BSO (bilateraalinen salpingo-ooforektomia)
- Vartijaimusolmuketutkimus indosyaniinivihreällä (ICG) kaikille potilaille
- Vatsapaidan poistoa suositellaan serööseissä karsinoomissa, karsinosarkoomissa ja erilaistumattomissa syövissä
- Leikkauksessa vältettävä kohdun sisällön pääsyä vatsaonteloon
- Kohtumanipulaattorin käyttö sallittu. Sen käyttö ei vähennä tautivapaata aikaa tai kokonaiselinaikaa4
- Avoleikkaus on suositeltavaa, jos metastaaseja esiintyy kohdun ja imusolmukkeiden ulkopuolella
- Kohdunkaulan stroomaan levinneessä syövässä ei suositella laajempaa kohdunpoistoleikkausta, jos normaalilla kohdunpoistolla päästään tautivapaaseen leikkaustulokseen
- Huuhtelunäytelöydös ei vaikuta levinneisyysmääritykseen, mutta se vaikuttaa uusiutumisriskiin
- Munasarjojen säästämistä voidaan harkita premenopausaalisilla alle 45-vuotiailla naisilla, joilla on low-grade endometrioidi syöpä (St 1A1 tai IA2 low grade, POLEmut/MMRd/NSMP ER+)
- jos munasarjat säästetään, suositellaan munatorvien poistoa
- munasarjojen säästämistä ei suositella, jos potilas kuuluu korkean riskin syöpäsukuun munasarjasyövän suhteen (BRCA, Lynch, korkean rintasyöpäriskin suku)
- Restaging-operaatiosta on hyötyä korkean keskitason riskin tai korkean riskin syövässä, jos leikkauksella on vaikutusta liitännäishoitoon
- Levinneessä taudissa (stage III-IV) leikkauksesta on hyötyä, mikäli päästään tautivapaaseen leikkaustulokseen. Pyritään kirurgiseen sytoreduktioon. Suurentuneet imusolmukkeet poistetaan, ei systemaattista imusolmukkeiden poistoa.
- Jos potilas ei sovellu yleiskunnon vuoksi standardikirurgiaan, voidaan harkita vaginaalista kohdunpoistoa, sädehoitoa (eksteri/braky) tai hormonaalista hoitoa.
Vartijaimusolmuketutkimus
- vartijaimusolmuketutkimusta suositellaan kaikille potilaille, joilla on kohtuun rajoittunut tauti
- ICG (indosyaniinivihreä) -menetelmä on suositeltavin
- injisoidaan kohdunkaulaan limakalvon alle ilman vastusta klo 3 ja klo 9.
- uusintainjektiota suositellaan, jos vartijaimusolmuketta ei ensimmäisellä kerralla löydetä
- jos vartijaimusolmuketta ei löydetä, suositellaan tehtäväksi ko. puolen lantion imusolmukkeiden systemaattinen poisto. Preoperatiivisesti matalan riskin taudissa pelvisestä lymfadenektomiasta voi pidättäytyä.
- jos vartijaimusolmukkeet eivät löydy kummaltakaan puolelta ja kyseessä on korkean riskin tauti, para-aortaalilymfadektomiaa voi harkita pelvisen lymfadenektomian lisäksi
- jos leikkauksen aikana todetaan lantion imusolmukemetastaasi, systemaattista lantion imusolmukkeiden poistoa on vältettävä; sen sijaan suurentuneet imusolmukkeet on poistettava ja para-aortaalista staging-leikkausta on harkittava
- ICG (indosyaniinivihreä) -menetelmä on suositeltavin
- imusolmukemetastaaseiksi luetaan sekä makro- (>2 mm) että mikrometastaasit (>0.2-2 mm ja/tai >200 solua, pN1(mi))
- yksittäisten tuumorisolujen (ITC, ≤0.2 mm ja ≤200 solua, pN0(i+)) prognostinen merkitys on vielä epäselvä
- vartijasolmukkeiden ultrastaging parantaa mikrometastaasien löytymistä. Yhteneväistä suositusta leikemääristä ja -tasoista ei ole. ESGO/ESTRO/ESP suosittelee kaksi leiketasoa 50 mikrom – 250 mikrom välein (HE-värjäykset ja immunohistokemia = sytokeratiini).
Adjuvanttihoito
Matala riski: Ei adjuvanttihoitoa.
- FIGO 2023 st IA1m, kaikki molekulaariluokat
- FIGO 2023 st IA2-IA3m POLE+, MMRd tai NSMP low grade ER+ endometroidi
- FIGO 2023 st IBm POLE+ endometroidi
- FIGO 2023 st ICm POLE+ tai MMRd endometroidi
- FIGO 2023 stIIm (IIA, IIB, IIC) POLE+endometroidi
Keskitasoinen riski: Suositellaan vaginaalista brakyterapiaa: alle 60-vuotiaat voidaan jättää hoitamatta.
- FIGO 2023 st IBm MMRd tai NSMP: low grade ER+
- FIGO 2023 st IIAm NSMP: low grade ER+
- FIGO 2023 IICm MMRd, myometrium inv+, ei cx stroomainv, ei runsasta LVI
Vaginaalisen brakyterapian toteutus:
- käytetään mielellään emättimen sylinteriä
- korkea-annosbrakyterapiassa annetaan emättimen ylimpään kolmannekseen 21-24 Gy 3-4 fraktiona 0.5 mm syvyyteen aplikaattorin pinnasta
Korkea keskitason riski: ulkoinen pelvinen sädehoito. Vaginaalinen brakyterapia on vaihtoehto erityisesti, jos vartijasolmukkeet on poistettu ja ovat puhtaat. Adjuvanttihoidosta voidaan myös pidättäytyä, jos vartijasolmuketutkimus on tehty, ei ole laajaa LVI:ta ja histologia on low grade.
- FIGO 2023 st IIAm MMRd endometrioidi
- FIGO st IIBm MMRd tai NSMP low grade ER+ endometroidi
- FIGO 2023 st IICm MMRd cx invaasio tai huomattava LVI
Ulkoisen sädehoidon toteutus:
- sädehoito aloitettava 6 viikon sisällä leikkauksesta
- IMRT /VMAT -tekniikat suositeltavimpia menetelmiä
- CTV sisältää lantion imusolmukkeet, parametriumin ja emättimen ylimmän osan
Korkea riski: ulkoinen sädehoito (toteutus kuten yllä) + kemoterapia; vaihtoehtona pelkkä kemoterapia, kemoterapia ja brakyterapia; immunoterapiaa (ICI) yhdistettynä kemoterapiaan potilaille FIGO 2023 st IIIm-IVAm MMRd-populaatiossa voi harkita.
-
- FIGO 2023 st Ia2m, IA3m tai IBm NSMP high grade ja/tai ER- ja/tai p53mut
- FIGO 2023 st IIm (IIA, IIB, IIC) NSMP high grade ja/tai ER- ja/tai p53mut
- FIGO 2023 st IIIm (IIIA, IIIB, IIIC) MMRd, NSMP low grade ja ER+, NSMP high grade ja/tai ER-, p53mut
- FIGO 2023 st IVAm MMRd, NSMP low grade ja ER+, NSMP high grade ja/tai ER- tai p53mut
FIGO 2023 st IIImPOLEmut ja IVAm POLEmut: moniammatillisen kokouksen käsittelyn jälkeen voidaan pidättäytyä korkean riskin syövän liitännäishoidosta
“Uncertain risk” -ryhmissä (esim. IA1m NSMP high grade ja/tai ER- tai p53abn ja ICm NSMP high grade ja/tai ER- tai p53abn; sekä IIIm/IVAm POLEmut) ei ole riittävää näyttöä adjuvanttihoidosta.
Levinneen tai uusiutuneen taudin hoito
- Immunologinen hoito (ICI) yhdistettynä kemoterapiaan ja ylläpitohoito kemoterapian jälkeen5 6 7
- standardi kemoterapia on 6 sykliä karboplatin + paklitakseli
Ensimmäinen linja (levinnyt tauti st III/IV, aiempi adjuvanttihoito sallittu):
- MMRd: Kemoterapia (karboplatiini + paklitakseli) + ICI (dostarlimabi, pembrolitsumabi, durvalumabi) ja ICI ylläpitohoito
- MMRp: Karboplatiini + paklitakseli + *ICI ja ylläpitohoito ICI ± **PARPi
- HER2+: kemoterapia (karboplatin + paklitakseli) + trastutsumabi (HER2+)
- matala-asteisissa ER-positiivisissa: hormonihoito; progestiinit (MPA, megestrol asetaatti), vaihtoehtona aromataasi-inhibiittorit ja tamoksifeeni
*ICI mahdollinen **PARPi mahdollinen
Toinen linja (uusiutunut tauti platinahoidon jälkeen)
- ICI-naiiville: Pembrolitsumabi + lenvatinibi (MMRp) tai pelkkä ICI (dostarlimabi), (MMRd), kemoterapiaan yhdistettynä pembrolitsumabi (MMRp, jos platinasta yli 12 kk)
- Jos aiemmin ICI: Platina-kemoterapia, doksorubisiini, viikko-paklitakseli, HER2+ trastusumabin lisääminen karboplatin + paklitakseli hoitoon tai hormoniterapia
Paikallinen uusiutuma: EBRT ± brachyterapia ± kemoterapia
- uudelleensädetyksessä harkitaan tapauskohtaisesti brakyterapiaa.
Levinnyt syöpä, immunologinen hoito (Suomen käytäntö)
- MMRd, MMRp
- Dostarlimabi 500 mg, paklitakseli 175 mg/m2 ja karboplatiini AUC5 iv 3vk välein x 6 jatkaen dostarlimabi 1000 mg iv 6 vk välein ad 3 vuotta.9
- EMA on hyväksynyt dostarlimabin myös MMRp-potilaille. Dostarlimabi on tarkoitettu käytettäväksi yhdistelmähoitona karboplatiinin ja paklitakselin kanssa primaarisen pitkälle edenneen tai uusiutuneen kohdun limakalvon syövän ensilinjan hoitoon aikuispotilaille, joille harkitaan systeemistä hoitoa.
- Dostarlimabi on tarkoitettu myös käytettäväksi monoterapiana (MMRd) / (MSI-H) -tyyppisen, uusiutuneen tai pitkälle edenneen kohdun limakalvon syövän hoitoon aikuispotilaille, kun syöpä on edennyt aiemman platinaa sisältävän hoito-ohjelman aikana tai sen jälkeen, myös karsinosarkooma
- Pembrolitsumabi 200 mg, paklitakseli 175 mg/m2 ja karboplatiini AUC5 iv 3 vk välein x 6 jatkaen pembrolitsumabi 200 mg kolmen vk välein tai 400 mg kuuden viikon välein, ei karsinosarkooma.
- EMA hyväksynyt pembrolitsumabin yhdistettynä karboplatinin ja paklitakselin kanssa primaaristi levinneen tai uusiutuneen kohdun limakalvosyövän hoitoon ensilinjassa ja jatkuen ylläpitohoitona sytostaattien jälkeen
- Pembrolitsumabi monoterapiana on tarkoitettu aikuisille sellaisten seuraavien kasvaimien hoitoon, joihin liittyy mikrosatelliitti-instabiliteetti (MSI-H) tai puutteellinen DNA:n kahdentumisvirheiden korjausmekanismi (MMRd)
- Dostarlimabi 500 mg, paklitakseli 175 mg/m2 ja karboplatiini AUC5 iv 3vk välein x 6 jatkaen dostarlimabi 1000 mg iv 6 vk välein ad 3 vuotta.9
- MMRp
- Pembrolitsumabi 200 mg iv 3 vk välein tai 400 mg 6 vk välein + lenvatinibi 2 x 10 mg po/vrk10
- Pembrolitsumabi yhdistelmänä lenvatinibin kanssa on tarkoitettu edenneen tai uusiutuneen endometriumkarsinooman hoitoon aikuisille, joilla tauti on edennyt aiemmin missä tahansa tilanteessa annetun platinapohjaisen hoidon aikana tai sen jälkeen ja jotka eivät sovellu saamaan parantavaa leikkaus- tai sädehoitoa.
- EMA hyväksynyt myös ensilinjaan durvalumabin yhdessä sytostaattihoidon kanssa jatkuen durvalumabi ja olaparibi ylläpitona sytostaatin jälkeen edenneen tai uusiutuneen MMRp kohdun limakalvosyövän hoitoon. Lisäksi durvalumabi solusalpaajahoitoon yhdistettynä ja jatkuen solusalpaajahoidon jälkeen ylläpitohoitona on hyväksytty MMRd kohdun limakalvosyövän hoitoon. Toistaiseksi olaparibille ei ole haettu Kela-korvattavuutta. Durvalumabilla ei ole HTA-käsittelyä.
- Pembrolitsumabi 200 mg iv 3 vk välein tai 400 mg 6 vk välein + lenvatinibi 2 x 10 mg po/vrk10
Fertiliteetin säästävä hoito8
- Voidaan harkita potilaalla, jolla atyyppinen hyperplasia / atyyppinen intraepiteliaalinen neoplasia (AH/EIN) tai noninvasiivinen st IA G1(-2) endometrioidi karsinooma ja raskaustoive.
- Erilaistumisaste on tärkeä riskitekijä: G1 reagoi hormonaaliseen hoitoon herkemmin, G2 histologiassa uusiumariski korkea 41%.
- Hoito järjestetään gynekologisen onkologin toimesta
- diagnoosi on varmistettava gynekologiseen patologiaan erikoistuneen patologin toimesta
- potilaat on tutkittava lapsettomuuspoliklinikalla ennen ja jälkeen fertiliteettiä säästävän hoidon
- Potilasta on informoitava, että fertiliteettiä säästävä hoito ei ole standardihoitoa
- potilaalla oltava toive säilyttää hedelmällisyys ja raskausmahdollisuus
- vaatii tarkkaa seurantaa ja toistuvia tutkimuksia
- ymmärrettävä, että lopulta kohdunpoisto on tarpeen, jos hoito epäonnistuu
- Diagnoosi ja taudin paikallinen levinneisyys varmennetaan hysteroskopialla ja fraktioidulla kaavinnalla, invaasio arvioidaan lantion MRI:llä ja transvaginaalisella ultraäänellä. Vartalon TT kaukolevinneisyyden poissulkuun.
- Hysteroskooppinen resektio ennen progestiinihoidon aloitusta on suotavaa.
- Hoidoksi resektion jälkeen suositellaan kohdunsisäistä levonorgestreeli-kierukkaa yhdistettynä po progestiiniin tai GnRH-analogiin.
- Medroksiprogesteroniasetaatin (MPA) annossuositus 400-600mg/vrk
- Hoitovaste arvioidaan 3-4 kk ja 6 kk kuluttua hysteroskopialla, histologisella näytteellä ja UÄ tutkimuksella
- hoitovaste tulee saavuttaa 6-12 kk:ssa, max 15 kk sisällä
- täydellinen vaste → suositellaan raskautta 6 kk sisällä
- lähete infertiliteettiklinikkaan; raskauden induktio ei lisää syövän uusiutumista
- jos vastetta, mutta potilas haluaa siirtää raskautta → ylläpitohoitona matala-annoksinen syklinen progestiini tai kohdunsisäinen hormonikierukka
- potilasta informoitava taudin uusimisen riskistä (19.2-33.8 %)
- evaluaatio 3-6 kk välein kliinisen statuksen, endometriumnäytteen ja vaginaalisen ultraäänitutkimuksen avulla
- jos epänormaali vuoto tai poikkeava ultraäänilöydös, tehtävä hysteroskopia ja otettava endometriumnäyte
- ei hoitovastetta tai progressio → standardi kirurginen hoito
- Synnytyksen jälkeen suositellaan kohdun ja sivuelimien poistoa johtuen suuresta uusiutumisriskistä
- Munasarjojen säästämistä voidaan harkita riippuen potilaan iästä ja geneettisestä syöpäriskistä
Lynch-seulonta ja geneettinen neuvonta
- MMR-proteiinien immunohistokemia (MLH1, PMS2, MSH2, MSH6) tehdään kaikista endometriumkarsinoomista.
- Jos MLH1/PMS2 puuttuu, tehdään MLH1-promootterin metylaatioanalyysi sporadisen taudin toteamiseksi (kuva 2).
- Ikäraja:
- <65-vuotiailla metylaatioanalyysi tehdään aina, jos MLH1/PMS2 puutos todetaan.
- ≥65-vuotiailla metylaatioanalyysi voidaan jättää tekemättä, ellei ole kliinistä tai sukuhistoriaan liittyvää epäilyä Lynch-syndroomasta.
- Jos löydös viittaa Lynch-syndroomaan, potilas ohjataan perinnöllisyyslääketieteen yksikköön geneettiseen neuvontaan ja ituradan mutaatiotestaukseen.
- Lynch-syndrooman kantajille suositellaan kirurgista profylaksiaa (hysterektomia ja BSO) 40-45 vuoden iässä.
- Geeniperäisen riskin tunnistaminen on tärkeää myös sukulaisille suunnattujen ehkäisy- ja seulontaohjelmien kannalta.
Kirjallisuusviitteet
Kohtusarkoomat
Päivitetty 26.2.2025.
- Kohdun pahanlaatuisista kasvaimista 3-9% on kohtusarkoomia:
- leiomyosarkooma (LMS, 60%)
- low grade ja high grade endometriaalinen stroomasarkooma (ESS, 30%)
- adenosarkooma (AS, 5%, mukaan lukien korkean riskin AS-SO = adenosarkooma, jossa sarkoomakomponentti vallitsevana)
- erilaistumaton kohdun sarkooma (UUS, 5%)
- Kohtusarkoomien harvinaisuuden takia konsultoi hoitolinjoista yo-sairaalan gynekologista onkologia
- Tarvittaessa konsultoi yo-sairaalan sarkoomatyöryhmää harvinaisissa sarkoomatyypeissä
Levinneisyystutkimukset
- Preoperatiivisesti lantion MRI ja vartalon TT
- Jos diagnoosi tulee postoperatiivisesti, tehdään vartalon TT
- Kasvainmerkkiaine LD
| Aste | Määritelmä |
| Leiomyosarkooma (C54.21) ja endometriaalinen stroomasarkooma (C54.22) | |
| I | Kasvain rajoittuu kohtuun |
| IA | Koko ≤ 5 cm |
| IB | Koko > 5 cm |
| II | Kasvain on levinnyt lantioon |
| IIA | Kohdun sivuelimiin |
| IIB | Muihin lantion kudoksiin |
| III | Kasvain on levinnyt vatsaonteloon/retroperitoneaalisesti |
| IIIA | Yhteen paikkaan |
| IIIB | Kahteen tai useampaa paikkaan |
| IIIC | Lantion ja/tai para-aortaalisiin imusolmukkeisiin |
| IV | Kasvain on levinnyt rakkoon/peräsuoleen tai lantion ulkopuolelle |
| IVA | Leviäminen virtsarakkoon ja/tai peräsuoleen |
| IVB | Kaukaiset etäpesäkkeet |
| Adenosarkooma (C54.29) | |
| I | Kasvain rajoittuu kohtuun |
| IA | Ei invasoi myometriumia |
| IB | Invaasio ≤ myometriumin puolivälin |
| IC | Invaasio > myometriumin puolivälin |
| II | Kasvain on levinnyt lantioon |
| IIA | Kohdun sivuelimiin |
| IIB | Muihin lantion kudoksiin |
| III | Kasvain on levinnyt vatsaonteloon/retroperitoneaalisesti |
| IIIA | Yhteen paikkaan |
| IIIB | Kahteen tai useampaa paikkaan |
| IIIC | Lantion ja/tai para-aortaalisiin imusolmukkeisiin |
| IV | Kasvain on levinnyt rakkoon/peräsuoleen tai lantion ulkopuolelle |
| IVA | Leviäminen virtsarakkoon ja/tai peräsuoleen |
| IVB | Kaukaiset etäpesäkkeet |
Hoito
Ensileikkaus
- kohdun ja kohdun sivuelinten poisto
- levinneisyysasteessa I voidaan harkita munasarjojen jättämistä premenopausaalisella
- LMS
- ESS LG ja AS pienet tuumorit (< 2 cm, ikä < 45v)
- pienet, paikalliset ESS LG: konservatiivinen fertiliteetin säästävä hoito harkittavissa
- UUS, ESS HG ja AS-SO: munasarjojen poisto aina suositeltavaa
- huuhtelunäyte vatsaontelosta
- suurentuneiden tai makroskooppisesti epäilyttävien imusolmukkeiden poisto
- kasvainnäytteestä hormonireseptorimääritys (ER, PR)
- LMS: mikäli kasvain on paloiteltu/morselloitu ensivaiheen leikkauksessa, uusintalaparoskopiaa tulee harkita levinneisyyden arvioimiseksi ja tautimuutosten poistamiseksi (upstaging 15-28%:ssa)
Liitännäishoidot
- radikaalisti leikatut, levinneisyysaste I (kohtuun rajoittunut): jatkohoitona on seuranta
- liitännäishoitoja voidaan harkita annettavaksi, mikäli kohtu on paloiteltu tai morselloitu (LMS)
- uusiutumariski 20%
- kohdun paloittelu/morsellointi lisää vatsaontelonsisäisen (lantio, peritoneaalinen) uusiutuman riskiä 44% vs9%
- ESS LG ja AS levinneisyysaste I: jatkohoitona seuranta
- 2-5 vuoden hormonaalista liitännäishoitoa voi harkita
Solunsalpaajahoito
- LMS (adjuvanttihoito)
- doksorubisiini tai gemsitabiini-dosetakseli
- doksorubisiini on kombinaatiohoitoja paremmin siedetty
- ylläpitona solunsalpaajahoidon jälkeen voi harkita hormonaalista lääkitystä ER/PR- positiivisessa kasvaimessa
- ESS HG, AS-SO, UUS: ifosfamidi-doksorubisiini, doksorubisiini, gemsitabiini-dosetakseli
Hormonaaliset hoidot
- ESS LG ja AS: adjuvanttihoitona levinneisyysaste ≥II taudeissa (aromataasi-inhibiittori, GnRh-analogit, fulvestrantti, keltarauhashormoni)
- jos tauti etenee hormonihoidon aikana, vaihdetaan toiseen hormonihoitoon
- jos tauti etenee useamman hormonihoidon läpi: (ifosfamidi-)doksorubisiini, gemsitabiini-dosetakseli
- Tamoksifeeni on kontraindisoitu
Ulkoinen sädehoito
- voidaan harkita tapauskohtaisesti kaikissa kohtusarkoomissa (esim. jos invaasio cervixiin, seroosaan tai parametrioihin tai tuumori rupturoituu leikkauksessa)
- sädehoito (annos 50.4 Gy) ei paranna kohtusarkoomien eloonjäämisennustetta, mutta vähentää paikallisen uusiutuman riskiä
Uusiutuneen ja edenneen taudin hoito
- LMS, ESS ja AS:
- määritä hormonireseptorit (ER, PR) viimeistään tässä vaiheessa
- yksittäisten etäpesäkkeiden operatiivinen poisto
- hormonihoito: aromataasi-inhibiittori, keltarauhashormoni
- solunsalpaajat:
- edennyt tai inoperaabeli (mitattava kasvain) LMS: 1. linjassa hyväkuntoisille doksorubisiini-trabektediini x 6 ja ylläpitohoito trabektediinillä ad 17 sykliä, jos ei progressiota
- levinneessä taudissa voi harkita debulking leikkausta, jos saadaan sytostaattivastetta ja arvioidaan päästävän optimaaliseen leikkaustulokseen R = 0
- uusiutumassa samat sytostaatit kuin ensilinjassa, yleensä yksittäiset solunsalpaajat
- LMS: myöhemmissä linjoissa voidaan harkita esim. trabektediinia, gemsitabiinia, dakarbatsiinia tai temotsolamidia, vinorelbiiniä tai patsopanibia
- UUS: solunsalpaajahoidot, ks. ensilinja (hormonihoidosta ei yleensä hyötyä)
- Palliatiivinen sädehoito 20-30 Gy: etäpesäkkeet kantavissa luissa, aivojen etäpesäkkeet, tukkivat hengitystiepesäkkeet, kivun hoito
- Paikallisesti edennyt, levinnyt tai leikkaushoidon ulkopuolella oleva tuumori, jossa todettu NTRK fuusiogeeni ja muut hoidot tehottomia: larotrektinibi tai entrektinibi
Kirjallisuusviitteet
Epiteliaalinen munanjohdin-, munasarja- ja vatsakalvonsyöpä ja rajalaatuiset kasvaimet
Diagnoosikoodit: C56.71, C56.72, C56.73, C56.79, C57.0, peritoneaalikarsinoosi C57.8, STIC D07.3
Päivitetty 24.7.2025.
Levinneisyystutkimukset
Diagnostiset tutkimukset
- ultraääni/vartalon TT/MRI ja PET-TT yksilöllisen tarpeen ja harkinnan mukaan
- CA 12-5, HE4, CEA, albumiini
- Jos todetaan hypoalbuminemia (<30), on suositeltavaa antaa neuvonta ravitsemuksen tehostamisesta jo lähettävän yksikön toimesta
FIGO munasarjasyövän levinneisyysluokittelu (2014)
| FIGO Stage | Kuvaus |
|---|---|
| IA | Tuumori rajoittuu toiseen ovarioon, intakti kapseli, ei syöpäsoluja tuumorin pinnalla, negatiivinen sytologia |
| IB | Tuumoria molemmissa ovarioissa, muutoin kuin IA |
| IC | Tuumoria joko toisessa ovariossa tai molemmissa ovarioissa
IC1: Tuumori puhjennut leikkauksessa IC2: Kapselin ruptuura ennen leikkausta tai syöpäsoluja ovarion pinnalla IC3: maligni askites tai huuhtelunäyte |
| IIA | Tuumori ulottuu (tai implantteja) kohtuun ja/tai munatorviin |
| IIB | Tuumori levinnyt lantiossa muualle kuin yllä mainittuihin |
| IIIA | Positiiviset retroperitoneaaliset imusolmukkeet ja/tai mikroskooppinen leviäminen lantion ulkopuolelle |
| IIIA1 | Vain positiiviset imusolmukkeet
IIIA1(i): metastaasit ≤ 10 mm IIIA1(ii): metastaasit > 10 mm |
| IIIA2 | Mikroskoopppisen ekstrapelviset metastaasit peritoneumilla ± positiiviset retroperitoneaaliset imusolmukkeet |
| IIIB | Makroskooppiset, ekstrapelviset, peritoneaaliset metastaasit ≤ 2 cm ± positiiviset retroperitonealiset imusolmukkeet. Sisältää myös maksan tai pernan kapseliin (ei parenkyymiin) ulottuvat metastaasit |
| IIIC | Makroskooppiset, ekstrapelviset, peritonealiset metastaasit > 2 cm ± positiiviset retroperitonealiset imusolmukkeet. Sisältää myös maksan tai pernan kapseliin (ei parenkyymiin) ulottuvat metastaasit |
| IVA | Pleuraneste, jossa maligni sytologia |
| IVB | Maksan ja pernan parenkyymimetastaasit, metastaasit vatsaontelon ulkopuolisiin elimiin (sisältää nivusen imusolmukkeet ja imusolmukkeet, jotka sijaitsevat vatsaontelon ulkopuolella) |
Hoito
Primäärileikkaus (PDS)
- Tavoitteena optimaalinen leikkaustulos = ei jäännöskasvainta=R0 (tai maksimaalinen sytoreduktio/jäännöskasvain <1cm =R1)
- Voidaan tyytyä R2 leikkaustulokseen tilanteessa, jossa tuumori iso ja potilas oireinen eikä neoadjuvanttihoitoa pystytä toteuttamaan
- Kohdun, kohdun sivuelinten, vatsapaidan, ja umpilisäkkeen poisto (musiineissa tuumoreissa tai mikäli umpilisäke on poikkeava)
- Suoli-, vatsakalvo- ja parenkyymielinten resektiot/poistot tarvittaessa
- Huuhtelunäytteiden ja kudosnäytteiden ottaminen vatsaontelosta lantion vatsakalvolta, parakoolisista sulkuksista ja palleankaarista.
- Jos näytteitä ei ole primaarileikkauksessa otettu, katsotaan restaging suositeltavaksi, vaikka se ei muuttaisikaan adjuvanttihoitoa
- Lantion ja para-aortaalisten imusolmukkeiden poisto (LND):
| Imusolmukestaging (lantion ja para-aortaalialueen lymfadenektomia) tulee suorittaa | Imusolmukestagingia (lantion ja para-aortaalialueen lymfadenektomia) ei suositella |
|---|---|
| Levinneisyysasteissa I-II, kaikki muut epiteliaaliset histologiat (low ja high-grade seroosi, high grade endometrioidi, kirkassoluinen, karsinosarkooma, musiini infiltratiivinen) paitsi musiini ekspansiilinen ja low grade endometrioidi |
|
-
- Levinneisyysasteissa I-II staging levinneisyyden selvittämiseksi
- ei ole tarpeen levinneisyysasteen I musinoosissa taudissa (expansile-tyyppi), eikä low grade endometrioidissa munasarjasyövässä (imusolmukemetastasointiriski n. 2-3%)
- ei ole tarpeen, jos sattumalta todetaan STIC (incidental STIC), mutta peritoneum stagingia suositellaan mieluiten mini-invasiivisesti
- vatsaontelon huuhtelunesteen sytologia, peritoneumbiopsiat lantiosta, parakoolisesti ja palleasta, vähintään infrakoolisen omentin resektio, mahdollisen jäljellä olevan adneksin poisto
- sattumalta löytyneen STIC-löydöksen jälkeen suositellaan testattavaksi iturata BRCA1/2-geenimutaatioiden ja perinnöllisyyslääkärin harkinnan mukaan myös muiden korkean penetranssin geenimutaatioiden suhteen
- Suositus korkean syöpäalttiuden (esim geneettisen alttiuden potilaat kuten BRCA1/2-mutaationkantajat) RRSO-leikkauksen suorittamiselle:
- Vatsaontelon sytologia ensin
- Vatsaontelon huolellinen tarkastelu, tarvittaessa peritoneumbiopsiat jos havaitaan poikkeavuutta (ei rutiinibiopsioita)
- Munatorvea ja munasarjaa ympäröivän peritoneumin poisto, IP-ligamentin katkaisu minimissään 2 cm ovariosta
- Munatorvet on tutkittava SEE-FIM protokollalla
- Mikäli todetaan STIC, mutta negatiivinen sytologia => yllä kuvattua staging-operaatiota ei suositella (poikkeavien löydösten esiintymisen todennäköisyys käytännössä 0 %). Mikäli sytologia on positiivinen, yllä kuvattu peritoneumstaging tulee suorittaa. Erityisesti BRCA1-mutaation kantajilla tulee harkita myös kohdunpoistoa.
- STIC-löydöksissä potilasta on informoitava peritoneaalikarsinoosin riskistä (5v riski 10.5% vs no-STIC 0.3%; 10v riski STIC 27.5% vs no-STIC 0.9%). STIC-potilaille on tarjottava pitkäaikaista seurantaa, jonka modaliteetista tai toteuttamisesta ei ole konsensusta
- Levinneisyysasteissa III-IV, radiologisesti tai kliinisesti poikkeavat / kookkaat imusolmukkeet poistetaan, ei tarvita systemaattista lymfadenektomiaa
- Levinneisyysasteissa I-II staging levinneisyyden selvittämiseksi
- Leikkausyksikössä täytyy olla riittävä kokemus leikkausten suorittamisesta ja leikkaajana gynekologinen onkologi. Suositellaan ESGOn laatukriteereiden noudattamista ja moniammatillista arviointia (Minimissään >20 sytoreduktiivista leikkausta/vuosi)
- Suoli-, vatsakalvo- tai parenkyymielinresektioissa sekä ultraradikaalileikkauksissa leikkaus on tarvittaessa tehtävä yhteistyössä muiden kirurgian erikoisalojen kanssa.
- BRCA1 ja -2 testaus (somaattinen ja/tai iturata) tulee tehdä primääritutkimuksena kaikista uusista ( ei-musiineista) epiteliaalisista munasarjasyövistä
- MMR-proteiinien ilmentymistä suositellaan tutkittavaksi endometrioideissa ja kirkassolukarsinoomissa (Lynchin syndrooman poissulkemiseksi)
- BRCA1 ja -2 testauksen lisäksi tuumorin HRD-status tulee määrittää diagnoosivaiheessa
- Työryhmä suosittelee patologian laboratorioissa munatorvien tarkkaa histopatologista tutkimusta (SEE-FIM), mikäli leikkauksessa todetaan high grade seroosi tauti munasarjoissa tai peritoneumilla munatorvien ollessa makroskooppisesti normaalit
- Leikkaustapa: ESGO-suosituksen mukaan laparotomia. Nykyisin sekä robotti- ja laparoskopia-avusteisesti munasarjasyöpäleikkauksia tehdään sekä primääri että intervalli leikkauksina hyvin raportoiduin tuloksin, mutta ESGO-suositukseen yltävä näyttö niistä vielä puuttuu. ESGO:n suosituksen mukaan laparoskooppista kirurgiaa voidaan käyttää restaging-leikkauksissa.
Fertiliteettiä säästävä leikkaus (FSS)
- Unilateraalinen s-o-ektomia ja täydellinen kirurginen staging
- ESMO-ESGO-konsensus 2019: Voi harkita low-grade stage IA (seroosi, endometrioidi tai musiini ekspansiilinen alatyyppi)-taudeissa
- Stage IC (FIGO 2014): FSS on hyväksyttävä IC1 tuumoreissa (puolet residiiveistä on isoloituja jäljelle jätetyn ovarion uusiutumia, jotka voidaan hoitaa kirurgialla). Stage IC2, StageIC3 ja gradus 3 taudeissa uusiutumisriski on korkea ja uusiutumat ovat usein ovarion ulkopuolisia ja näin vaikeammin hoidettavia. Näissä tapauksissa FSS ei ole suositeltava.
Neoadjuvanttihoito
- niissä tilanteissa missä radiologisten tutkimusten (CT, MRI, PET-CT) ja/ tai diagnostisen laparoskoskopialöydöksen perusteella ei ole mahdollista päästä primäärileikkauksella optimaaliseen leikkaustulokseen R0 (tai R1), suositellaan valittavaksi primäärihoidoksi neoadjuvantti kemoterapia.
- Neoadjuvanttihoitoa puoltaa ohutsuolen meson laaja syvä infiltraatio, laaja ohutsuolen karsinoosi, vatsalaukun/duodenumin infiltraatio, haiman pään/keskiosan infiltraatio, tautia truncus celiakuksessa, maksavaltimoissa tai vasemmassa a. gastricassa, useita maksan parenkyymimetastaaseja, keuhkometastaaseja, huonosti resekoitavat imusolmukemetastaasit tai aivometastaasit
- Neoadjuvanttihoitoa on myös syytä harkita potilaille, joilla on tuore tromboosi, korkea ikä, raihnaisuus, useita kroonisia sairauksia, huono ravitsemustila (matala albumiini), ja primaarileikkaus katsotaan mahdolliseksi esimerkiksi kuntoutustoimenpiteiden tai ravitsemustilanteen paranemisen jälkeen
- Neoadjuvanttihoitoa voi erityisesti harkita, kun taudin levinneisyys on FIGO stage IVB (EORCT-55971 tutkimuksessa OS hyöty vs. PDS, mutta pois lukien resekoitavissa olevat nivus- ja kardiofreeniset imusolmukkeet, maligni pleuraneste ilman vahvaa näyttöä pleurametastaaseista)
- paklitakseli+karboplatiini 3 viikon välein 3–4 hoitokertaa.
- mikäli biokemiallinen vaste on hyvä (Ca 12-5 laskenut/puoliintunut) ja radiologisessa /laparoskooppisessa vastearviossa on tavoitettu RECIST kriteerein PR /CR, potilas leikataan ensilinjan leikkausperiaatteita noudattaen pyrkimyksenä optimaalinen leikkaustulos (R0)
- Intervallileikkauksen (IDS) onnistumisen (=optimaalinen leikkaustulos) todennäköisyyden arvioinnissa voi käyttää apuna laskennallista KELIM-arvoa (CA12-5 elimination constant K)
Ensilinjan solunsalpaajahoito
- Liitännäishoitona annetaan muissa paitsi stage IA low grade seroosi, G1-2 endometrioidi, G1 -2 musiineissa (expansiilinen) taudeissa edellyttäen, että primaarileikkauksen ja kuvantamisen perusteella voidaan määritellä tauti stage IA:ksi
- Sattumalta löytyneessä STIC-muutoksessa ei suositella solusalpaajahoitoa, mikäli kirurginen/peritoneaalinen staging on tehty
- Varhaisvaiheen taudissa potilaat saavat paklitakselia ja karboplatiinia, minimimäärä kolme sykliä, mutta high grade serooseissa tai stage IC, kuusi sykliä
- Stage II-IV low grade seroosissa OC:ssa tulee harkita sytostaattihoidon jälkeistä hormonaalista hoitoa 5 vuoden ajan
- Levinneessä taudissa (FIGO III-IV) paklitakselin ja karboplatiinin (PK) yhdistelmä 3viikon välein kuusi hoitokertaa, vasteen ja harkinnan perusteella useammat syklit mahdollisia
- Levinneessä taudissa uusiutumisriski on korkea ja mahdollisuutta sytostaattihoidon jälkeiseen ylläpitohoitoon tulisi harkita ja pohtia jokaisen potilaan kohdalla; ylläpitohoidon vaihtoehtoja ovat bevasitsumabi, olaparibi, bevasitsumabin ja olaparibin yhdistelmä sekä niraparibi. Näiden ylläpitohoitojen käyttöindikaatioita käydään läpi alempana.
- Pelkkä karboplatiini, jos suorituskyky tai perussairaus estävät paklitakselin käytön
- Viikottainen karboplatiini (AUC2) ja paklitakseli (60mg/m2) voi olla myös hyväksyttävä vaihtoehto
- Intraperitoneaalinen ja HIPEC –hoito on suositeltavaa vain niihin suunnatuissa kliinisissä tutkimuksissa.
Bevasitsumabi ensilinjan hoidossa
- Suositellaan käytettäväksi ICON7-tutkimuksen mukaan:
- korkean riskin potilaille: kun levinneisyysaste on IIIB tai IIIC ja leikkaustulos on ollut suboptimaalinen (jäännöskasvaimen koko > 1 cm) tai levinneisyysaste on IV
- Bevasitsumabin liittämistä ensilinjan hoitoon voidaan harkita myös, mikäli sytostaattivaste todetaan riittämättömäksi:
- jos laskennallinen KELIM-arvo todetaan epäsuotuisaksi (<1) tai
- jos IDS-leikkausnäytteissä todetaan huono histopatologinen vaste (esim. arvioituna 3-portaisella CRS eli chemotherapy response scorella)
- Annostelu: Sytostaattihoitoon liitettynä ja sen jälkeen ylläpitohoitona annoksella 7,5 mg/kg (ICON7) tai 15 mg/kg (GOG218) iv kolmen viikon välein, hoidon kokonaiskesto 15 kk, aloitus aikaisintaan neljä viikkoa leikkauksesta
- Voidaan antaa myös neoadjuvanttihoidossa ennen ja jälkeen intervallileikkausta edellyttäen vähintään 4 viikon taukoa leikkaukseen
Parp-inhibiittorit ensilinjassa; Olaparibi, Niraparibi, Rukaparibi
Olaparibi
- SOLO-1 tutkimusnäytön perusteella suositellaan ensilinjassa ituradan BRCA-mutaation omaaville potilaille, joilla todetaan levinnyt stage III-IV high grade munasarja- munatorvi- tai peritoneum- lähtöinen karsinooma, olaparibi ylläpitohoitoa, edellyttäen että on saatu vaste platinapohjaiselle hoidolle (merkitsevä PFS etu; 7v OS 67% olaparibilla vs 46.5% plasebolla). Ylläpitohoitoaika on tutkimuksessa ollut kaksi vuotta, mutta hoitoa on mahdollista jatkaa pidempäänkin, mikäli hoitava lääkäri arvioi potilaan siitä hyötyvän (esim 2 vuoden kohdalla on todettavissa edelleen syöpämuutoksia).
- PAOLA1-tutkimuksen näytön perusteella (merkitsevä PFS etu; 5v OS 65.5% olaparibilla vs 48.4% plasebolla): Kun potilaalle on aloitettu/suositeltu bevasitsumabi-hoitoa, olaparibi suositellaan liitettäväksi hoitoon sytostaattihoidon jälkeen ylläpitovaiheessa 2 vuoden ajaksi seuraavin edellytyksin:
- Kyseessä pitkälle edennyt (FIGO-levinneisyysasteet III ja IV) korkean pahanlaatuisuusasteen epiteelistä munasarja-, munanjohdin‑ tai primaaria peritoneaalista syöpä, ja kun hoitovaste (täydellinen tai osittainen) on säilynyt platinapohjaisen solunsalpaajahoidon ja bevasitsumabin yhdistelmällä annetun ensilinjan hoidon jälkeen ja syöpään liittyy positiivinen HRD-status (homologous recombination deficiency) määriteltynä joko BRCA1/2-mutaation ja/tai genomin epävakauden perusteella
- Kliinistä HRD-testausta suositellaan tehtäväksi kaikille uusille munasarjasyöpäpotilaille BRCA1/2-testauksen rinnalla
Niraparibi
- Uusimman tutkimusnäytön perusteella (Prima-tutkimus) kaikki potilaat hyötyvät merkittävästi ensilinjassa niraparibi-ylläpitohoidosta (verrattuna plaseboon; merkitsevä PFS-etu; ei OS-etua), mikäli heillä on pitkälle edennyt (FIGO-levinneisyysasteet III ja IV) korkean pahanlaatuisuusasteen epiteelinen munasarja-, munanjohdin‑ tai primaari peritoneaalinen syöpä, ja hoitovaste (täydellinen tai osittainen) on säilynyt platinapohjaisen solunsalpaajahoidon jälkeen riippumatta siitä onko heillä somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin positiivinen HRD-status.
- Ituradan BRCA1/2-mutaatio ennustaa niraparibin tehoa ensilinjassa parhaiten, sitten positiivinen HRD-status (mukaan lukien somaattinen BRCA1/2-mutaatio), mutta näiden biomarkkereiden puuttuessakin niraparibi pidensi merkitsevästi tautivapaata aikaa verrattuna plaseboon. Niraparibi-ylläpitohoidon kesto ensilinjassa 3 vuotta.
Rukaparibi
- Athena-Mono-tutkimuksessa rukaparibi-monoterapia/ylläpitohoito pidensi tautivapaata elinaikaa (PFS) merkitsevästi verrattuna plaseboon, kun potilailla oli pitkälle edennyt (FIGO-levinneisyysasteet III ja IV) korkean pahanlaatuisuusasteen epiteelinen munasarja-, munanjohdin‑ tai primaari peritoneaalinen syöpä, ja hoitovaste (täydellinen tai osittainen) on säilynyt platinapohjaisen solunsalpaajahoidon jälkeen riippumatta siitä onko heillä somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin positiivinen HRD-status. Hoidon teho oli kuitenkin paras HRD-positiivisessa ryhmässä. OS tuloksia ei ole vielä saatavilla. Rukaparibi-hoidon kesto oli tutkimuksessa 2 vuotta. OS-dataa ei ole vielä käytettävissä.
Vaihtoehdot levinneen stage III-IV munasarjasyövän ylläpitohoidoksi ensilinjan sytostaattihoidon jälkeen
| BRCA1/2-mutaatio tai HRD | HRD-negatiivinen / HRP |
|---|---|
Aina PARP-inhibiittori
|
|
Valintaan vaikuttavat tekijät:
|
Valintaan vaikuttavat tekijät:
|
Korvattavuus ensilinjassa:
Edenneet (stage III-IV) high grade taudit
- Ensilinjassa ylempi erityiskorvattavuus olaparibi-monoterapialle, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio, sekä ylempi erityiskorvattavuus olaparibin ja bevasitsumabin yhdistelmälle, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin HRD-positiivisuus.
- Ylempi erityiskorvattavuus (1.7.2022 lähtien) niraparibi-monoterapialle, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin HRD-positiivisuus.
- 1.6.2025 lähtien peruskorvaus (40%) rukaparibi-monoterapialle ensilinjassa, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin HRD-positiivisuus.
Käytännössä (korvattavuuden näkökulmasta) ylläpitohoitovaihtoehdot ensilinjassa
- BRCA1/2-mutaatio (aina PARPi): olaparibi-monoterapia, olaparibin ja bevasitsumabin yhdistelmä tai niraparibi tai rukaparibi
- Positiivinen HRD-status, mutta BRCA1/2-negatiivinen tauti (aina PARPi): olaparibin ja bevasitsumabin yhdistelmä tai niraparibi tai rukaparibi (aina peruskorvaus)
- Negatiivinen HRD-status: bevasitsumabi tai ei mitään
Uusiutuneen taudin hoito
- Pelkän merkkiaineen nousun perusteella ei ole syytä aloittaa uusiutuman hoitoa (erityistilanteissa yksittäisen uusiutuman kirurginen poistoharkinta)
- Kuvantamistutkimukset vain oireiden perusteella ja harkiten, jos merkkiaine nousee > 2-kertaiseksi normaaliin ylärajaan verrattuna, vähintään kaksi määritystä, väli yli kuukausi
- Kuvantamistutkimuksista luotettavin on PET-TT uusiutuneen taudin diagnostiikassa
Sekundaarinen sytoreduktiivinen kirurgia platinaherkässä uusiutumassa
- Uusiutuneessa taudissa kirurgiaa on harkittava tarkoin valikoituneessa populaatiossa edellyttäen, että optimaalinen leikkaustulos voidaan saavuttaa.
- 3 RCT aiheesta; GOG-213, jonka tulos oli negatiivinen ja DESKTOP III, joka osoitti PFS ja OS-edun kirurgiaryhmässä, mikäli päästään täydelliseen sytoreduktioon (=R0-tulos). Samoin PFS-etu kiinalaisessa SOC1-tutkimuksessa tarkoin valikoiduilla potilailla (platinaherkkä yli 6kk ja positiivinen iModel-score).
- DESKTOP III-tutkimuksen sisäänottokriteerit: 1. uusiutuma ja 6kk platinahoidon päättymisestä (75% platinavapaa-aika oli yli 12kk). Kaikilla randomisoiduilla potilailla positiivinen AGO score:
- ECOG 0, ascites ≤ 500 mL, and optimaalinen (R0) leikkaustulos primaaristi.
- Leikkaushoidon vaikuttavuus ennusteeseen on todettu parhaimmaksi silloin kun primäärileikkaus on ollut optimaalinen, uusiutuminen tapahtuu >12 kk primäärihoidosta, ei askitesta, kasvain on yksittäinen tai oligometastaattinen, ei karsinoosia, eikä todeta parenkymaalisia tai vatsaontelon ulkopuolisia kasvaimia
- Harkitse herkemmin kirurgista interventiota, mikäli kyseessä on uusiutunut musinoosi, low grade seroosi tai kirkassoluinen histologia
Kemoterapia
Platinasensitiivinen tauti/platina on vaihtoehto
- Mikäli BRCA- tai HRD-status ei ole tiedossa, se on testattava uusiutuman yhteydessä
- Mikäli tauti ei ole progredioinut platinapohjaisen hoidon aikana, kyse on platinasensitiivisestä uusiutumasta, mutta platinavapaa intervalli on prediktiivinen platinavasteelle uusiutumassa
- platinasensitiivisissä uusiutumissa aloitetaan karboplatiini yhdistettynä pegyloituun liposomaaliseen doksorubisiiniin (PLD), taksaaniin tai gemsitabiiniin huomioiden potilaan aiempien hoitojen haitat (karboplatiini yhdistettynä pegyloituun liposomaaliseen doksorubisiiniin saattaa olla ensisijainen vaihtoehto)
- platinakombinaation kesto 6 sykliä
Bevasitsumabi platinasensitiivisen uusiutuneen taudin hoidossa
- Sytostaattihoitoon liitettynä (liposomaalinen doksorubisiini-karboplatiini (ensisijainen), paklitakseli-karboplatiini, gemsitabiini-karboplatiini) ja sen jälkeen ylläpitohoitona.
- Uusiutuneessa taudissa tutkimuksissa käytetty annos on ollut 15 mg/kg (tai sytostaattihoidon aikana 10mg/kg PLD-karboon yhdistettynä). Ylläpitohoitoa jatketaan progressioon tai haittoihin asti. Bevasitsumabia voidaan MITO16B-MaNGO-tutkimuksen mukaan käyttää uudelleen uusiutumassa ilman tehon menetystä, vaikka potilas olisi bevasitsumabia jo ensilinjassa saanut.
Parp-inhibiittorit platinasensitiivisessä uusiutumassa
- Aiemman tutkimusnäytön mukaisesti PARP-inhibiittorit (olapaja ribi, niraparibi ja rukaparibi) pidentävät tautivapaata aikaa ylläpitohoitona, mikäli platinahoidolle on saavutettu vaste uusiutuneessa taudissa, ja niitä voi suositella annettavaksi, vaikka ituradan BRCA-mutaatiota ei todeta
- Uusiutuneessa taudissa ylläpitohoitoa jatketaan progressioon (tai haittoihin) asti.
- Mikäli PARP-inhibiittorihoitoa ei ole käytetty ensilinjassa, se on ensisijainen vaihtoehto platinaherkässä uusiutumassa ylläpitohoidoksi monoterapiana, mikäli potilaalla on somaattinen tai ituradan BRCA1/2-mutaatio tai tuumori on HRD-positiivinen, ja platinalle on saatu täydellinen tai osittainen vaste.
- Korvattavuus
- Ylempi erityiskorvaus olaparibille; Toisen linjan/platinaherkän uusiutuneen taudin ylläpitohoito, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio.
- Ylempi erityiskorvattavuus niraparibille (1.7.2022 alkaen): Toisen linjan/platinaherkän uusiutuneen taudin ylläpitohoito, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin positiivinen HRD-status.
- Peruskorvaus rukaparibille (1.6.2025 alkaen): Toisen linjan/platinaherkän uusiutuneen taudin ylläpitohoito, kun on saatu osittainen tai täydellinen vaste platinahoidolle ja on todettu somaattinen tai ituradan BRCA1/2-mutaatio tai tuumorin positiivinen HRD-status.
Platinaresistentti tauti/platina ei ole vaihtoehto
- mikäli progressio todetaan platinapohjaisen hoidon aikana, kyse on platinaresistentistä uusiutumasta
- High grade serooseista kannattaa viimeistään tässä vaiheessa määrittää FRα-kasvainstatus, mikäli se ei ole tiedossa (ks seuraava kohta)
- High grade seroosissa platinaresistentissä taudissa mirvetuksimabi-soravtansiini (kauppanimi Elahere®; Suomessa myyntilupa, mutta FIMEA/Palko-käsittely kesken) on ensisijainen vaihtoehto (OS hyöty osoitettu verrattuna single-sytostaattihoitoon), mikäli kasvaimessa todetaan positiivinen FRα-kasvainstatus, mikä määritellään solukalvon kohtalaiseksi (2+) ja/tai voimakkaaksi (3+) värjäytymiseksi 75 %:ssa elinkykyisistä kasvainsoluista immunohistokemiallisessa tutkimuksessa (IHC) tähän käyttöön tarkoitetulla CE-merkityllä in vitro diagnostisella (IVD) laitteella arvioituna.
- Muutoin ensisijaisena vaihtoehtona on Bevasitsumabi sytostaattihoitoon liitettynä (viikko-paklitakseli, topotekaani, PLD). Annos joko 10 mg/kg kahden viikon välein tai 15 mg/kg 3 viikon välein. Hoitoa jatketaan progressioon/haittoihin asti. Hoitoa voidaan jatkaa monoterapiana (joko sytostaatti yksin tai bevasitsumabi yksin) toistaiseksi, mikäli toksisuus estää yhdistelmähoidon
- Edellä mainittujen vaihtoehtojen jälkeen tai jos ne eivät tule kyseeseen: yksittäiset solunsalpaajat: ensisijaisesti viikko-paklitakseli tai vaihtoehtoisesti PLD, topotekaani, dosetakseli, epirubisiini, etoposidi, gemsitabiini, irinotekaani, ifosfamidi, kapesitabiini, oksaliplatiini, vinorelbiini (nab-paklitakselia voidaan käyttää, jos paklitakselille allergia/paklitakselia ei voi enää käyttää) TAI lääketutkimus, mikäli siihen on mahdollisuus
- hoito jatkuu niin kauan kuin kliinistä hyötyä havaitaan eikä toksisuus ole esteenä
Hormonihoito
- Aromataasi-inhibiittori-, tamoksifeeni, GnRH-analogi tai fulvestrantti –hoidot voivat tulla kyseeseen etenkin low-grade-taudeissa harkinnan perusteella
- Low grade taudeissa voidaan käyttää ylläpitohoitona solunsalpaajahoidon jälkeen
Uusiutunut low grade seroosi munasarjasyöpä, kun edellä mainitut standardihoidot on käytetty
- Uusiutuneessa low grade seroosissa taudissa (platinahoitoa jo saaneilla) on osoitettu PFS-hyöty trametinibilla verrattuna single-sytostaatteihin tai hormonaalisiin hoitoihin riippumatta BRAF-mutaatiostatuksesta (ei KELA-korvattavuutta, vaatii potilaskohtaisen luvan esim sairaalan lääketyöryhmältä lääkeluovutukseen)
Palliatiivinen hoito
- uusiutuneessa taudissa potilas tulisi ohjata riittävän ajoissa palliatiiviseen konsultaatioon
- palliatiivinen sädehoito (20-30Gy): etäpesäkkeet kantavissa luissa, aivojen etäpesäkkeet, tukkivat hengitystiepesäkkeet, kivun hoito
- leikkaukset: suolitukos
- stenttaus: hydronefroosi
- nestekertymien dreneeraukset: pleura, askites, nefrostoomat
- pahoinvoinnin ja kivun hoito
Rajalaatuiset kasvaimet
Primäärileikkaus
- kohdun, kohdun sivuelinten, ja vatsapaidanpoisto
- musiinissa umpilisäke, seroosissa vain poikkeava umpilisäke poistetaan
- jos fertiliteetin säästäminen on tarpeen, voidaan säästää kohtu ja terve adnex
- serooseissa kystaenukleaatio on hyväksyttävää, jos muutos on bilateraalinen. Tällöinkin suositellaan toisen puolen adnexin poistoa koska kystaenukleaation jälkeen residiiviriski on korkea, 40% luokkaa.
- jos toinen ovario on terve ja säästetään, jäävän ovarion biopsiointia ei suositella
- fertiliteetin säästävän leikkauksen jälkeen myöhemmin tehtävästä täydentävästä kohdun ja toisen adneksin poistosta ei ole ennusteellista hyötyä
- omentti poistetaan colon transversumin alapuoliselta osaltaan
- peritoneumbiopsiat otetaan kuten munasarjasyövässä
- imusolmukkeiden poisto ei ole tarpeen
Restaging rajalaatuisissa kasvaimissa
Restaging-operaatioista ei ole vaikutusta elinajan ennusteeseen, joten restaging-leikkausta on syytä harkita vain, jos kyseessä on seroosi mikropapillaarinen alatyyppi tai primaarileikkauksessa on tehty puutteellinen vatsaontelon tarkastelu (lähinnä peritoneumpinnat). Näyttö hyödystä mikropapillaarisen alatyypinkin kohdalla on kuitenkin vähäinen.
Kirjallisuusviitteet
Ei-epiteliaalinen munasarjasyöpä
Päivitetty helmikuussa 2024.
Levinneisyystutkimukset
- vartalon TT (nuorilla MRI)
- kasvainmerkkiaineet
- sukupienakasvaimet: inhibiini, AMH, CA12-5, AFP (E2, testo)
- SCCOHT: kalsium, NSE, CgA
- itusolukasvaimet: AFP, LD, hCG, hCG-B (E2, testo)
- sukupienakasvaimet: inhibiini, AMH, CA12-5, AFP (E2, testo)
Hoito
Sukupienakasvaimet
Ensileikkaus
- kohdun ja sivuelinten poisto, vatsapaidan poisto
- huuhde- ja kudosnäytteiden otto vatsaontelosta
- poikkeavien imusolmukkeiden poisto
- levinneessä taudissa maksimaalinen sytoreduktio
- Granulosasolukasvain: hedelmällisyyden säästävä leikkaus paikallisessa taudissa: adneksin poisto ja vatsaontelon levinneisyysnäytteet, endometriumbiopsia
- Sertoli-Leydigsolukasvain: hedelmällisyyden säästävä leikkaus paikallisessa, hyvin erilaistuneessa kasvaimessa (St IA, G1) mahdollinen, muilla valikoidusti
- Small cell carcinoma of the ovary of hypercalcemic type (SCCOHT): aina radikaalileikkaus, pelvinen ja para-aortaalinen lymfadenektomia
Liitännäishoito
Granulosasolukasvain
- Stage IA-IC1: ei liitännäishoitoa
- Stage IC2-3: BEP (bleomysiini-etoposodi-sisplatiini) x3, (>40v EP; bleomysiinin keuhkotoksisuus korostuu iän myötä), PK (paklitakseli-karboplatiini) x6 tai single-K [bleomysiini: keuhkofunktiotutkimukset ennen aloitusta]
- Stage II-IV: BEP x3, (> 40v EP) tai PK x6
Sertoli-Leydigsolukasvain
- Stage IA G1: ei liitännäishoitoa
- Stage I G2-IV: BEP x3-4, (>40v EP) tai PK x6
SCCOHT
- sisplatiini-etoposidi
Uusiutuneen taudin hoito
- leikkaus harkinnan mukaan, jos kasvainmuutokset poistettavissa (vatsaontelo, etäpesäkkeet maksassa, keuhkoissa, muissa elimissä)
- solunsalpaajahoito: PK, BEP, VAC (vinkristiini-daktinomysiini-syklofosfamidi), PVB (sisplatiini-vinblastiini-bleomysiini), VIP (etoposidi-ifosfamidi-sisplatiini), CAP (syklofosfamidi-doksorubisiini-sisplatiini), paklitakseli, dosetakseli, karboplatiini, syklofosfamidi, doksorubisiini, ifosfamidi
- hormonaaliset hoidot: aromataasi-inhibiittori, tamoksifeeni, leuproreliini, MPA
- GCT: bevasitsumabi (single)
- paikallinen sädehoito
Muuta
- Granulosasolukasvain St IA-B: leikkauksen jälkeen mahdollinen estrogeenihoito yksilöllisesti
Itusolukasvaimet
Ensileikkaus
- kohdun ja sivuelinten poisto
- jos raskaus toive, voidaan poistaa ainoastaan adneksi. Kohtu ja terve adneksi tai edes osa toisesta ovariosta voidaan säästää, vaikka kyseessä olisi levinnyt tauti
- vatsapaidan poisto
- huuhde- ja kudosnäytteiden otto vatsaontelosta
- poikkeavien imusolmukkeiden poisto
- levinneessä taudissa sytoreduktio
- nuorilla vältetään liian ekstensiivistä kirurgiaa (kemosensitiivinen syöpä)
Liitännäishoito
- BEP tai EP
Dysgerminooma
- Stage IA-B ei liitännäishoitoa, jos asianmukainen levinneisyysleikkaus tehty
- Stage IC: nuorilla voi harkita pelkkää seurantaa, jos asianmukainen levinneisyysleikkaus tehty
- Stage IC-IV: BEP x 3-4, (>40v EP)
Epäkypsä teratooma
- Stage IA G1: ei liitännäishoitoa
- Stage IA G2-3: voi harkita pelkkää seurantaa, jos asianmukainen levinneisyysleikkaus tehty, negatiiviset kasvainmerkkiaineet leikkauksen jälkeen
- Stage IB-IV: BEP x 3-4
Yolk sac –kasvain
- Stage IA: ei liitännäishoitoa (asianmukainen levinneisyysleikkaus, negatiiviset kasvainmerkkiaineet leikkauksen jälkeen)
- Stage IB-IV: BEP x 3-4
Embryonaalinen karsinooma
- StI-IV
Uusiutuneen taudin hoito
- leikkaus harkinnan mukaan
- BEP (tai sisplatiinin sijaan karboplatiini), EP, TIP (paklitakseli-ifosfamidi-sisplatiini) tai IP, VeIP (vinblastiini- ifosfamidi-sisplatiini), VIP, VAC, PK, paklitakseli-gemsitabiini, gemsitabiini-oksaliplatiini, dosetakseli. [Etoposidi-karboplatiini: St IB-III dysgerminoma, jos toksisuuden lievittäminen tarpeen]
- paikallinen sädehoito
- erityisesti dysgerminoma sädeherkkää
Muuta
- hormonaalista ehkäisyä voi käyttää
- ei estettä hormonikorvaushoidolle
Kirjallisuusviitteet
Trofoblastitaudit
Päivitetty 18.9.2025.
Trofoblastitautien luokittelu (WHO 2020)
| Tumor-like lesions | Exaggerated placental site reaction (benigni)Placental site nodule and plaque (benigni)
· Atypical placental site nodule (PSTT:n esiaste) |
| Abnormal (nonmolar) villous lesions | |
| Molar pregnancies (rypäleraskaudet)(hyperplastisia muutoksia) | Partial hydatidiform moleComplete hydatidiform mole
Invasive and metastatic hydatidiform mole |
| Gestational trophoblastic neoplasms(maligneja) | Epithelioid trophoblastic tumor (ETT)Placental site trophoblastic tumor (PSTT)
Mixed trophoblastic tumor Choriocarcinoma (istukkasyöpä) Choriocarcinoma combined with other germ cell elements |
Persistoivan matalan hCG-pitoisuuden tulkinnassa huomioitavaa
- Heterofiiliset vasta-aineet
- Voivat aiheuttaa väärän positiivisen S-hCG-tuloksen (pitoisuus tyypillisesti <150 ky/l).
- Virtsan hCG on negatiivinen (heterofiiliset vasta-aineet eivät suodatu virtsaan).
- Voidaan todentaa laboratoriomenetelmin (laimennossarja tai vasta-aineiden poisto) (HUSLAB-tutkimus 20561, S-Imm-Ong).
- Ektooppinen hCG-tuotanto
- Itusolukasvaimet, epiteliaaliset ja muut syövät
- Erittävät yleensä vapaata hCG-betaa.
- Tarvittaessa kuvantamistutkimukset (vartalon TT, aivojen ja aivolisäkkeen MRI)
- Aivolisäkkeen hCG:n kaltainen molekyyli
- GnRH stimuloi eritystä perimenopaussista alkaen.
- Eritys suppressoituu E-pillereillä (tarvittaessa 3 viikon hoitokokeilu)
- Munuaisten vajaatoiminta
- Familiaalinen tai nonfamiliaalinen korkea hCG
- Quiescent gestational trophoblastic neoplasia (GTN)
- Hitaasti kasvavat hyvin erilaistuneet synsytiotrofoblastin solut tuottavat non-hyperglykosyloitunutta hCG:tä.
- Ilmentymänä stabiili, matala S-hCG (yleensä 50-100 ky/l) vähintään 3 kk ilman todettavaa trofoblastitautia (kuvantaminen, kaavinta, hysteroskopia)
- Ilmaantuu yleensä rypäleraskauden jälkeen.
- Seuranta, jos ei merkkejä progressiosta
- Noin 20% progredioituu aktiiviksi trofoblastitaudiksi → hoito.
Levinneisyystutkimukset
Rypäleraskaus
- Thorax-rtg (huomioidaan riskipisteytyksessä) ja vaginaalinen kaikukuvaus
- Thorax-rtg:ssä metastasointiepäily → thoraxin TT (ei huomioida riskipisteytyksessä) ja metastasoinnin varmennuttua mahan TT ja pään MRI
Istukkasyöpä, ETT, PSTT, epäily korkean riskin postmolaarisesta GTN:sta, tautirelapsi
- Vartalon TT, lantion ja pään MRI
Hoito
Yleiset hoitoperiaatteet
- Rypäleraskaus hoidetaan kohdun imutyhjennyksellä. Rh(D)-negatiivisille potilaille annetaan anti-D-profylaksia. Kohdun imutyhjennyksen sijasta voidaan harkita kohdunpoistoa ja salpingektomiaa, jos potilaalla ei ole raskaustoivetta.
- Postmolaarinen GTN hoidetaan solunsalpaajilla. Kohdunpoisto ja salpingektomia tulee kyseeseen kun suurin tautimassa sijaitsee kohdussa. Terveet munasarjat on mahdollista säästää. Metastaasisuspektit lantion ja/tai para-aortaaliset imusolmukkeet poistetaan.
- ETT:n ja PSTT:n hoito on ensisijaisesti kirurginen.
Postmolaarinen GTN
- Kehittyy 15-20%:ssa täydellisistä ja 1-5%:ssa osittaisista rypäleraskauksista.
- Diagnostiset kriteerit:
-
- Stabiili S-hCG (≥4 arvoa ±10% vähintään 3 viikon aikana, esim. päivinä 1, 7, 14, 21)
- Nouseva S-hCG (+10% 2 kertaa peräkkäin vähintään 2 viikon aikana, esim. pv 1 vs. pv 7 ja pv 7 vs. pv 14)
- S-hCG koholla >6 kk kohdun imutyhjennyksen jälkeen
- Istukkasyöpä tai invasiivinen mola
- Etäpesäkkeitä
- Postmolaarinen GTN jaetaan matalan ja korkean riskin tauteihin riskipisteluokituksen avulla (taulukko 2).
Trofoblastitautien riskipisteluokitus (taulukko 2)
| Riskipisteet | 0 | 1 | 2 | 4 |
|---|---|---|---|---|
| Ikä (v.) | <40 | ≥40 | – | – |
| Edeltänyt raskaus | rypäleraskaus | keskenmeno | täysiaikainen | – |
| Hoidon aloitus edeltävän raskauden jälkeen (kk) | <4 | 4–6 | 7–12 | ≥13 |
| S-hCG ennen hoitoa (ky/l) | <103 | 103–104 | >104–105 | >105 |
| Suurin kasvain (cm) | <3 | 3–5 | >5 | – |
| Etäpesäkkeiden sijainti | keuhkot | perna, munuainen | suolisto | aivot, maksa |
| Etäpesäkkeiden määrä | 0 | 1-4 | 5-8 | >8 |
| Edeltänyt epäonnistunut solunsalpaajahoito | – | – | yksi lääke | lääkkeitä kaksi tai useampi |
Persistoivan ja uusiutuneen taudin hoito
Taulukko 3. Trofoblastitautien riskipisteluokitus (FIGO 2000), pisteiden summa:
- <7, matala riski
- ≥7, korkea riski
Matalan riskin tauti (riskipisteet 0-6)
- Suositellut monoterapiat
- Metotreksaatti 1 mg/kg (tai 50 mg) i.m. päivinä 1, 3, 5, 7 ja foolihappo 15 mg p.o. 30 h kunkin metotreksaattiannoksen jälkeen päivinä 2, 4, 6, 8. Toistetaan 14 päivän välein.
- Metotreksaatti 0,4 mg/kg/päivä (max 25 mg/päivä) i.v. 5 peräkkäisenä päivänä. Toistetaan 14 päivän välein.
- Aktinomysiini-D 0,5 mg i.v. 5 peräkkäisenä päivänä 14 päivän välein
- Aktinomysiini-D 1,25 mg/m2v. 14 päivän välein (ei istukkasyövässä eikä metrotreksaatille resistentissä taudissa, kts. alla)
- Aktinomysiini-D aiheuttaa enemmän sivuvaikutuksia kuin metotreksaatti (alopesia, pahoinvointi, myelosuppressio, ekstravasaatiossa pehmytkudosvaurio). Aktinomysiini-D:n käyttö tulee parhaiten kyseeseen maksa- ja munuaisviassa.
- Solunsalpaajia annetaan kunnes S-hCG on normalisoitunut ja 2-3 sykliä sen jälkeen.
- Ei-metastasoineessa matalan riskin taudissa voidaan solunsalpaajahoidon sijasta harkita uutta kohdun imutyhjennystä, erityisesti 20-39-vuotiailla potilailla ja kun riskipisteitä on ≤4.
Korkean riskin tauti (riskipisteet ≥7)
- Hoito
- Ensisijainen hoito on yleensä EMACO (etoposidi, metotreksaatti, aktinomysiini-D, syklofosfamidi, vinkristiini). Vuodon ja metabolisten komplikaatioiden välttämiseksi voidaan antaa low-dose etoposidi-sisplatiinia x 1-3 ennen EMACO-hoitoon siirtymistä.
- Aivometastaaseissa vaihtoehtoina metotreksaatin annoksen nosto, intratekaalinen metotreksaatti, neurokirurgia, sädehoito
- Solunsalpaajia annetaan kunnes S-hCG on normalisoitunut ja 2-4 sykliä sen jälkeen, ultrakorkean riskin taudissa (riskipisteet ≥13) 3-4 sykliä.
- Kuvantaminen toistetaan hoidon päätyttyä (myöhempää vertailua varten, jos tauti uusiutuu)
Persistoivan ja uusiutuneen taudin hoito
- Uudet kuvantamistutkimukset ennen hoidon vaihtoa.
- Metotreksaatille resistentissä matalan riskin taudissa (taulukko 3) voidaan pyrkiä remissioon aktinomysiini-D:llä, jos S-hCG on ≤1000 ky/l. Pitoisuuden ollessa suurempi suositellaan EMACO-hoitoa.
- Yhdistelmähoito on suositeltava myös seuraavissa tilanteissa:
- histologisesti todettu metastasoinut istukkasyöpä
- hoitoa edeltävä S-hCG >410000 ky/l
- todettu metastaaseja tai istukkasyöpä ja hoitoa edeltävä S-hCG >150000 ky/l.
- Jos EMACO:lla ei saavuteta remissiota korkean riskin taudissa, EMAEP (etoposidi, metotreksaatti, aktinomysiini-D, sisplatiini) voi osoittautua tehokkaaksi. Solunsalpaajille resistenteissä taudeissa käytetään salvage-hoitoja, jotka ovat solunsalpaajien, sädehoidon ja kirurgisen hoidon erilaisia yhdistelmiä. Ne suunnitellaan potilaskohtaisesti, koska tietoa parhaista hoitomenetelmistä ei ole.
Taulukko 3. Metotreksaattiresistenssin kriteerit matalan riskin postmolaarisessa GTN:ssa.
| Primääri resistenssi | Hoidon vaihto, jos S-hCG nousee 2 syklin jälkeen. Jos S-hCG on stabiili (<10% muutos), annetaan 3. sykli ja hoito vaihdetaan sen jälkeen, jos S-hCG edelleen stabiili. |
| Hankittu resistenssi alkuvaiheen vasteen jälkeen | Stabiili S-hCG kahden syklin jälkeen (<10% muutos) tai nousu vähintään 2 viikon aikana.
Harkitse persistoivan matalan hCG-pitoisuuden erotusdiagnostisia tutkimuksia. |
Muuta
- Angiografista embolisaatiota voi harkita kirurgisen hoidon sijasta esim. emätinmetastaasin aiheuttamassa akuutissa vuodossa.
ETT:n ja PSTT:n diagnostiikka ja hoito
- Epäiltävä jos S-hCG matala suhteessa kuvantamisessa todettuun tautivolyymiin.
- Tuumorin biopsia tai resektio suositeltava histologisen diagnoosin saamiseksi.
- Levinneisyystutkimukset: vartalon TT, lantion ja pään MRI
- Hoidon suunnittelussa ei käytetä riskipisteytystä vaan FIGO 2000 levinneisyysluokitusta yhdistettynä riskitekijöihin (stage I, kohtuun rajoittunut; stage II, leviäminen adnekseihin tai emättimeen; stage III, leviäminen keuhkoihin; stage IV, kaikki muu levinneisyys)
- Levinneisyysaste I ja aika < 4 vuotta edellisen raskauden päättymisestä: hoitona hysterektomia ja salpingektomia.
- Muissa tilanteissa suositellaan leikkauksen jälkeen 12-16 viikon kestoista EMAEP-hoitoa. Sytostaattihoitoa voidaan harkita myös levinneisyysasteessa I vaikka aika olisi < 4 vuotta edellisen raskauden päättymisestä, jos kasvaimessa todetaan muita riskitekijöitä, kuten syvä invaasio, nekroosia tai runsaasti mitooseja (>5 per 10 HPF).
- Kuvantaminen hoidon jälkeen (hCG epäluotettava).
- Hoito on ensisijaisesti kirurginen (kohdunpoisto ja salpingektomia, mahdollisuuksien mukaan metastaasien resektio). Solunsalpaajia käytetään liitännäishoitona metastasoituneissa kasvaimissa ja harkinnan mukaan paikallisissa korkean riskin kasvaimissa. Tärkein paikallisten kasvainten ennusteellinen riskitekijä on pitkä aika (> 4 v.) edellisen raskauden päättymisestä. Ensisijainen solunsalpaajahoito on yleensä EMAEP.
Trofoblastitautien seuranta
- Täydellinen rypäleraskaus
- S-hCG määritetään 2 vrk:n kuluttua kohdun imutyhjennyksen jälkeen ja sitten 2 viikon välein kunnes arvo on ollut 3 kertaa peräkkäin normaali. Sen jälkeen hCG-seurantaa jatketaan kuukauden välein 6 kuukauden ajan.
- Osittainen rypäleraskaus
- S-hCG-seurantaa jatketaan kohdun imutyhjennyksen jälkeen 2 viikon välein kunnes arvo on ollut 2 kertaa peräkkäin normaali.
- Seuranta-aikana tulee huolehtia luotettavasta raskaudenehkäisystä. E-pilleriehkäisyn voi aloittaa heti kohdun imutyhjennyksen jälkeen.
- Seuraavien raskauksien alussa tulee tehdä kohdun kaikukuvaus (uusiutumisriski yhden rypäleraskauden jälkeen 1,3% ja kahden rypäleraskauden jälkeen 15%). Synnytyksen jälkeen istukka tutkitaan histologisesti ja äidin S-hCG määritetään 6 viikon kuluttua.
- Postmolaarinen GTN
- Matalan riskin tauti: S-hCG 2 viikon välein 3 kuukauden ajan, sitten kuukauden välein vuoden ajan
- Korkean riskin tauti: S-hCG viikon välein 6 viikon ajan, sitten kuukauden välein vuoden ajan, sitten 6-12 kuukauden välein ad 5 v
- Raskautta ei suositella vuoden sisällä kemoterapian päättymisestä.
- ETT, PSTT
- S-hCG viikon välein 6 viikon ajan, sitten kuukauden välein vuoden ajan, sitten 6-12 kuukauden välein ad 10 v.
- Vatsan MRI ja thoraxin TT 6 kk välein 2 vuoden ajan, sitten vuosittain 5 vuoden ajan.
Kirjallisuusviitteet
Perinnöllinen syöpäalttius
Päivitetty 30.3.2025.
Geneettisiin syndroomiin liittyvien gynekologisten kasvainten riski naisilla
| Syndrooma | Geeni | Gyn.syöpä | Riski | Keskeiset muut syövät |
|---|---|---|---|---|
| Homologiseen rekombinaatioon liittyvät geenimutaatiot | BRCA1
BRCA2 RAD51C RAD51D PALB2 BRIP1 |
Munasarja | BRCA1: 44% (10-21% 50 v. mennessä)
BRCA2: 17% (2-3% 50 v. mennessä) RAD51C: 11% RAD51D: 13% PALB2: 5% (ad 10% jos merkittävä munasarjasyövän sukuanamneesi) BRIP1: 10-15% |
BRCA1: rinta (65-85%), haima (2.3%), maha (0.7%)
BRCA2: rinta (45-85%), haima (2.3%), maha (3.5%) RAD51C: rinta (21%) RAD51D: rinta (20%) PALB2: rinta (53%), haima (2-3%) |
| Lynch | MLH1
MSH2/EPCAM MSH6 PMS2 |
Munasarja
Kohtu |
MLH1 10%, MSH2 17%, MSH6 13% (3-4% 40 v. mennessä), PMS2 epävarma
MLH1 43%, MSH2 57%, MSH6 46%, PMS2 13% (0-3% 40 v. mennessä) |
Paksusuoli (10-82% mutaatiosta riippuen), mahalaukku (3-13% mutaatiosta riippuen), muut <10% (sappitiet, ohutsuoli, virtsatiet, haima, aivot) |
| Peutz-Jeghers | STK-11 | Munasarja 1
Kohtu Kohdunkaula 2 |
18-21%
9% 10% |
Rinta (45-50%), paksusuoli (39%), maha (29%), ohutsuoli (13%), haima (11-36%), keuhkot (15-17%) |
| Cowden | PTEN | Kohtu | 19-28% | Rinta (35-50%), kilpirauhanen (3-38%), munuainen (~30%), paksusuoli (9%), melanooma (5-10%) |
| Li-Fraumeni | P53 | Munasarja
Kohtu |
Suuruus ei tiedossa | Pehmytkudos- ja luusarkooma, rinta-, aivo-,lisämun.ca, akuutti leukemia (90% sairastuu johonkin syöpään) |
| PPAP | POLD1, POLE | Kohtu | Suuruus ei tiedossa | Paksusuoli (suuruus ei tiedossa) |
| DICER1 3 | DICER1 | Munasarja 4
Kohdunkaula 5 |
Suuruus ei tiedossa | Pleuropulmonary blastoma, struuma ja kilpirauhassyöpä, munuaisen kystinen nefrooma, Wilmsin tuumori ja anaplastinen sarkooma |
| HLRCC | FH | Kohdun leiomyoomat | 77% | Ihon leiomyoomat (76%), munuaissyöpä (10-16%) |
1 Benigni SCTAT (sex cord tumor with annular tubules); 2 Adenoma malignum; 3 Kasvaimet ilmaantuvat yleensä lapsuudessa; 4 Sertoli-Leydiginsolutuumori; 5 Embryonaalinen rabdomyosarkooma; PPAP, polymerase proofreading–associated polyposis; HLRCC, hereditary leiomyomatosis and renal cell cancer
Ensikäynti
Kun mutaatio on todettu, perinnöllisyyslääkärin käynnin jälkeen käynti oman alueen erikoissairaanhoidon naistentautien poliklinikalla asiaan perehtyneillä gynekologeilla, joille käynnit keskitetään.
- Informaatio geenimutaatioon liittyvistä syöpäriskeistä.
- Informaatio riskiä pienentävistä tekijöistä.
- Jokaisella naisella on oma tapansa reagoida epävarmuuteen.
- Yksilöllinen lähestyminen.
- Huomion kiinnittäminen henkiseen tukemiseen, informaatio vertaistuesta, kursseista.
- Informaatio mihin ottaa yhteyttä, mikäli herää huolta.
- Informaatio iästä, johon mennessä suositellaan riskiä vähentävää kirurgiaa.
- Jatkoseuranta ja profylaktinen kirurgia alla olevan taulukon mukaisesti.
Gynekologisten kasvainten seuranta- ja hoitosuositukset geneettisissä syndroomissa
| Syndrooma | Seurantasuositus | Kirurginen profylaksia |
|---|---|---|
| Ensikäynti kun diagnoosi tehty | ||
| Homologiseen rekombinaatioon liittyvät geenimutaatiot,
Lynch |
Ensikäynnin jälkeen seuraava käynti kun potilas saavuttaa profylaktisen leikkauksen suositusiän, jolloin suunnitellaan leikkauksen ajankohta. Jos potilas ei ole valmis päättämään leikkauksesta, seuraavan käynnin ajankohta suunnitellaan yksilöllisesti, mutta rutiiniseurantaa ei suositella. | BRCA1: RRSO 35-40-vuotiaana
BRCA2: RRSO 40-45-vuotiaana RAD51C, RAD51D, PALB2, BRIP1: RRSO 45-50-vuotiaana PALB2: RRSO harkinnan mukaan 50-vuotiaana jos merkittävä munasarjasyövän sukuanamneesi Lynch: kohdunpoisto ja RRSO 40-45-vuotiaana |
| Peutz-Jeghers | UÄ ja papa vuosittain ≥18-20-vuotiailla | Yksilöllinen |
| Cowden | Ei rutiiniluonteista gynekologista seurantaa | Ei |
| Li-Fraumeni | Ei erillistä gynekologista seurantaa, jos sarkoomaseulonta järjestetty (mahan kuvantamiset) | Yksilöllinen |
| PPAP | UÄ ja CA125 ± endometriumbiopsia vuosittain ≥40-vuotiailla | Yksilöllinen |
| DICER1 | UÄ ± gyn. tutkimus vuosittain lapsuudesta 40-vuotiaaksi asti | Yksilöllinen |
| HLRCC | UÄ vuosittain ≥20-vuotiailla | Yksilöllinen |
RRSO, risk-reducing salpingo-oophorectomy
Muuta
Huomioitavaa BRCA1/2:ssa
- E-pilleriehkäisy pienentää munasarjasyövän riskiä eikä suurenna rintasyövän riskiä merkitsevästi.
- Munasarjasyövän riski on pieni, jos RRSO tehdään suositellussa iässä eikä STICiä todeta (20 v:n seurannassa BRCA1 1,5 %, BRCA2 0,2 %)
- katso suositus toteuttamistavasta osiosta Epiteliaalinen munanjohdin-, munasarja- ja vatsakalvosyöpä ja rajalaatuiset kasvaimet kohdasta Primäärileikkaus
- Premenopausaalisesti tehty RRSO todennäköisesti pienentää rintasyövän riskiä n. 50%.
- Hormonihoito on sallittu RRSO:n jälkeen.
- RRSO:n jälkeen ei tarvetta gynekologiselle seurannalle.
- RRSO on kirurgisen profylaksian standardi, salpingektomiaa ja myöhemmin tehtävää ooforektomiaa ei voi rutiinisti suositella.
Vahva munasarjasyövän ja/tai rintasyövän sukuanamneesi ilman todettua geenimutaatiota
- Potilas kutsutaan lähetteen perusteella vastaanotolle informaation antamista varten.
- Ei rutiiniseurantaa, RRSO tapauskohtaisesti.
- Pelkkä positiivinen rintasyövän sukuanamneesi ilman munasarjasyövälle altistavaa geenivirhettä ei assosioidu suurentuneeseen munasarjasyövän riskiin, jolloin vastaanottoa ei tarvita (palaute lähettävään yksikköön).
Geenitestaus syöpädiagnoosin jälkeen
- Epiteliaalinen munasarjasyöpä ja kohdunrunkosyöpä: kts. hoitoa koskevat kappaleet.
- Munasarjan Sertoli-Leydiginsolutuumoreissa ja kohdunkaulan embryonaalisessa rabdomyosarkoomassa tulee harkita ituradan DICER1-mutaatiotutkimusta (lähete Kliinisen genetiikan yksikköön).
Kirjallisuusviitteet
Gynekologisten syöpien seuranta
Päivitetty 18.1.2026.
Seurannan tarkoitus
- Potilaan psykososiaalinen tukeminen
- Yleisvoinnin ja terveyden tukeminen
- Seulontoihin kannustaminen
- kohdunkaulasyövän seulonta (HPV-riippuvat syövät, mm. ulkosynnytinsyöpä)
- mammografiaseulonta (rintasyöpä RR 1.3-4)
- ulosteen veren seulonta (paksu- ja peräsuolisyöpä RR 1.2-5.9)
- Hoitohaittojen havaitseminen ja hoito
- lymfadenektomian jälkeiset alaraajaturvotukset, vaihdevuosioireet, seksuaalineuvonnan tarve
- Varovaisuusperiaatteet hormonihoidon käytössä: kts. taulukko 1
- Taudin uusiutumisen toteaminen
- Hoidon laadun ja hoitotulosten arviointi
- Seulontoihin kannustaminen
Seurantakäyntien sisältö
- Esitiedot – onko syövän uusiutumiseen viittaavia oireita?
- Yleis- ja gynekologinen tutkimus
- Kohdunrunkosyöpä
- Rutiininomaista irtosolunäytettä ja kuvantamista ei voi suositella.
- Epiteliaalinen munasarjasyöpä
- CA125-seuranta ei johda oireettoman munasarjasyöpäpotilaan parempaan ennusteeseen, mutta potilaskohtaista harkintaa voidaan käyttää. Kuvantamistutkimukset harkiten, jos merkkiaine nousee >2-kertaiseksi normaalin ylärajaan verrattuna, vähintään kaksi määritystä, väli yli kuukausi.
- Rutiininomaista kuvantamista ei suositella.
Varovaisuusperiaatteet hormonihoidon käytössä gynekologisissa syövissä
Muissa kuin mainituissa tilanteissa ei ole syövästä johtuvia vasta-aiheita käytölle.
| Paikallinen hoito | |
| Kohtusarkoomat (erityisesti reseptoripositiiviset) |
|
| Endometrioidi munasarjasyöpä | |
| Sukupienakasvaimet | |
| Systeemihoito | |
| Kohdunrunkosyöpä stage III-IV |
|
| Kohtusarkoomat (erityisesti reseptoripositiiviset) | |
| Endometrioidi munasarjasyöpä | |
| Low grade seröösi munasarjasyöpä | |
| Seröösi rajalaatuinen munasarjakasvain | |
| Sukupienakasvaimet | |
Seurannan aikavälit
| Syöpä | Riski | Seurantaväli | |
|---|---|---|---|
| Ulkosynnytinsyöpä (levyepiteeli) |
Matala riski | Stage I-II, ei liitännäishoitoja | 1.-2. vuosi 6 kk välein 3.-5. vuosi 12 kk välein |
| Korkea riski | 1) Stage I-II ja liitännäishoito
2) Stage III-IV |
1.-2. vuosi 4 kk välein
3. vuosi 6 kk välein 4.-5. vuosi 12 kk välein |
|
| Emätinsyöpä | Matala riski | Stage I | 1.-2. vuosi 6 kk välein
3.-5. vuosi 12 kk välein |
| Korkea riski | Stage II-IV | 1.-2. vuosi 4 kk välein
3. vuosi 6 kk välein 4.-5. vuosi 12 kk välein |
|
| Vulvovaginaalinen melanooma | Matala riski | AJCC-luokat I, IIA, IIIA | 6-12 kk välein 5 vuoden ajan |
| Keskikorkea riski | AJCC-luokat IIB, IIC ja IIIB | Jos täydentävää LND ei ole tehty, nivusen uä 1.-2. vuosi 4–6 kk välein ja 3.-5. vuosi 6–12 kk välein.
CT-kuvaus 4–12 kk välein |
|
| Korkea riski | AJCC-luokat IIIC-D ja IV | PET/CT 4–12 kk välein | |
| Kohdunkaulasyöpä | Radikaalisti leikattu stage I levyepiteelikarsinooma tai usual type adenokarsinooma, ei liitännäishoitoja | 1. vuosi 6 kk välein
2. vuosi 12 kk välein 24 kk kohdalla exit-papa ja HPV-testi, jatkoseuranta kts. kuva 1. |
|
| Radikaalisti leikatut + liitännäishoito | 4 kk välein ad 2 v., 6 kk välein ad 3 v.
36 kk kohdalla exit-papa ja HPV-testi, jatkoseuranta kts. kuva 1. |
||
| Kemosädehoidetut | 4 kk välein ad 2 v., 6 kk välein ad 3 v. ja oire-pkl ad 5 v.
Alavatsan MRI 4 kk ja 12 kk, koko kehon PET-TT 8 kk. |
||
| Fertiliteetti säästäen leikatut | 1.-2. vuosi 4 kk välein (HPV-testi 4 kk, 12 kk ja 24 kk)
3. vuosi 6 kk välein Sitten oire-pkl ad 5 v. |
||
| Kohdunrunkosyöpä | Matala/epäselvä riski ‒ keskitason riski | Yksi käynti 6 kk, jonka jälkeen oire-pkl ad 3 v. | |
| POLEmut stage I-II, joka kuuluu ilman molekulaarista luokittelua vähintään korkean keskitason riskiin | Ensimmäinen käynti 6 kk, sitten vuosittain ad 3 v. ja oire-pkl ad 5 v. | ||
| Korkean keskitason riski ‒ Korkea riski ‒ Edennyt, metastaattinen | 1. vuosi 4 kk välein
2.-3. vuosi 6 kk välein Sitten oire-pkl ad 5 v. |
||
| Kohtusarkoomat | Matalan riskin histologia
(AS, ESS LG) |
Stage I: 1.-3. vuosi 6 kk välein, sitten oire-pkl ad 5 v.
Stage II-IV: 1. vuosi 4 kk välein, 2.-3. vuosi 6 kk välein, sitten oire-pkl ad 5 v. Kuvantaminen oireiden ja löydösten perusteella. |
|
| Korkean riskin histologia
(LMS, ESS HG, AS-SO, UES) |
1. vuosi 4 kk välein, 2.-3. vuosi 6 kk välein, sitten oire-pkl ad 5 v.
Vartalon TT kontrollikäyntien yhteydessä 3 vuoden ajan, sitten vuosittain ad 5 v. |
||
| Epiteliaalinen munasarjasyöpä | Matala riski | Stage IA-B low grade seröösi, G1-2 endometrioidi tai musinöösi karsinooma, asianmukainen levinneisyysleikkaus tehty, ei liitännäishoitoja | Yksi käynti 6 kk, jonka jälkeen oire-pkl ad 3 v. |
| Korkea riski | 1) High grade seröösi, G3 endometrioidi ja kirkassoluinen karsinooma stagesta riippumatta
2) Stage IC-IV low grade seröösi, G1-2 endometrioidi tai musinöösi karsinooma 3) Fertiliteetti säästäen leikatut |
1. vuosi 3 kk välein
2.-3. vuosi 6 kk välein Sitten oire-pkl ad 5 v. Ylläpitohoito (bevasitsumabi, PARPi) lasketaan mukaan seurantaan. |
|
| Munasarjan itusolukasvain | Huomioidaan, onko operoitu säästävästi vai radikaalisti.
Yleis- ja gynekologinen tutkimus 4 kk:n välein 2 ensimmäisen vuoden ajan ja sen jälkeen vuoden välein ad 5 v. Kasvainmerkkiaineiden (AFP, hCG, LDH) seuranta mikäli diagnoosivaiheessa koholla. Kuvantamistutkimukset vain oireiden ja kliinisen tutkimuksen/merkkiaineiden nousun perusteella. |
||
| Munasarjan sukupienakasvain | Yleis- ja gynekologinen tutkimus matalan riskin (varhaisvaiheen, early stage) potilaille 12 kk:n välein ja korkean riskin potilaille 6 kk:n välein ad 5 v.
Granuloosasolutuumoreissa seurannan kesto määräytyy yksilöllisesti huomioiden kasvaimen myöhäinen uusiutumistaipumus (mediaaniaika uusiutuman ilmaantumiseen 4-6 v.). Kasvainmerkkiaineiden (estradioli, inhibiini, AMH, testosteroni) seuranta mikäli diagnoosivaiheessa koholla (granuloosasolutuumoreissa inhibiini ja AMH lähtötilanteesta riippumatta). |
||
| Rajalaatuinen munasarjakasvain | Radikaali leikkaus (BSO) | Yksi käynti 6 kk | |
| Säästävä leikkaus (kystektomia tai unilateraalinen s-o-ektomia) | 1. vuosi 6 kk välein
2.-3. vuosi 12 kk välein |
||
| Noninvasiivisia implantteja | 1. vuosi 6 kk välein
2.-3. vuosi 12 kk välein Sitten seuranta avosektorilla ad 10 v. |
||
Kuva 1. Leikkauksella hoidetun kohdunkaulasyövän seurantaohjelma ennen oire-pkl:n seurantaan siirryttäessä

Trofoblastitautien seuranta
Täydellinen rypäleraskaus
- S-hCG määritetään 2 vrk:n kuluttua kohdun imutyhjennyksen jälkeen ja sitten 2 viikon välein kunnes arvo on ollut 3 kertaa peräkkäin normaali. Sen jälkeen hCG-seurantaa jatketaan kuukauden välein 6 kuukauden ajan.
Osittainen rypäleraskaus
- S-hCG-seurantaa jatketaan kohdun imutyhjennyksen jälkeen 2 viikon välein kunnes arvo on ollut 2 kertaa peräkkäin normaali.
Yleistä rypäleraskauksien seurannasta
- Seuranta-aikana tulee huolehtia luotettavasta raskaudenehkäisystä. E-pilleriehkäisyn voi aloittaa heti kohdun imutyhjennyksen jälkeen.
- Seuraavien raskauksien alussa tulee tehdä kohdun kaikukuvaus (uusiutumisriski yhden rypäleraskauden jälkeen 1,3% ja kahden rypäleraskauden jälkeen 15%). Synnytyksen jälkeen istukka tutkitaan histologisesti ja äidin S-hCG määritetään 6 viikon kuluttua.
Postmolaarinen gestationaalinen trofoblastineoplasia
- Matalan riskin tauti: S-hCG 2 viikon välein 3 kuukauden ajan, sitten kuukauden välein vuoden ajan
- Korkean riskin tauti: S-hCG viikon välein 6 viikon ajan, sitten kuukauden välein vuoden ajan, sitten 6-12 kuukauden välein ad 5 v.
- Raskautta ei suositella vuoden sisällä kemoterapian päättymisestä.
Epitelioidi trofoblastikasvain, istukkapedin trofoblastikasvain
- S-hCG viikon välein 6 viikon ajan, sitten kuukauden välein vuoden ajan, sitten 6-12 kuukauden välein ad 10 v. Seuranta kuvantamistutkimuksilla tulee kyseeseen, jos hCG oli primääristi normaali tai vain lievästi koholla.
Kirjallisuusviitteet
Elämänlaatu – muistilista gynekologista syöpää hoitaville ammattilaisille
Uusi, luotu 30.3.2025.
Maailman terveysjärjestön (WHO) määrittelee terveyden ”täydellisen fyysisen, psyykkisen ja sosiaalinen hyvinvoinnin tilaksi, ei pelkästään sairauden puuttumiseksi”
Muistilista on luotu elämänlaadun huomioimisen apukeinoksi gynekologisia syöpäpotilaita kohtaaville ammattilaisille. Eri kohtia voi käydä potilaan ja tämän läheisten kanssa läpi sitä mukaa, kun ne ovat ajankohtaisia – kaikkea ei tarvitse käydä kerralla läpi. Tärkeintä on, että ammattilainen muistaa ottaa asiat puheeksi, joskus useammankin kerran, tehdä tarvittavat interventiot ja ohjata potilaan tarvittaessa eteenpäin.
Henkinen tuki ja taloudelliset resurssit
- Tarjoa mahdollisuus moniammatilliseen keskusteluapuun, myös sosiaalityöntekijän kanssa
- Huomioi perhe; puoliso, lapset, läheiset
- Syöpään sairastuneen nettiterapia (Mielenterveystalo.fi), kts. läheteohjeet
- Ohjaa vertaistukeen
- Suomen Gynekologiset Syöpäpotilaat GySy ry:n vertaistuki
- paikalliset syöpäyhdistykset
- Ohjaa psykososiaaliseen tukeen
- Luoto – maksuton Syöpäjärjestöjen ammattilaisten tarjoama tuki
Vajaaravitsemus
- Erityisesti levinnyttä munasarjasyöpää sairastavilla ja leikkaushoitoja suunniteltaessa
- NRS-2002 seulonta
- Tarvittaessa lähete ravitsemusterapeutille, jos kohtalainen tai vakava vajaaravitsemuksen riski
Fertiliteetti
- Ota puheeksi
- ennen hoitoja, erityisesti jos vaikuttaa hoitomenetelmän valintaan (cervix-, ovario- ja endometriumkarsinooma)
- Huomioi realistinen raskaustoive
- hoitojen jälkeen, kun syöpä on hoidettu fertiliteettiä säästäen
- Raskauslupa, tarve lapsettomuushoitoihin tai tukilankaan
- Tarvittaessa lisääntymislääketieteen lääkärin konsultaatio ennen hoitoa ja hoitojen jälkeen
- ennen hoitoja, erityisesti jos vaikuttaa hoitomenetelmän valintaan (cervix-, ovario- ja endometriumkarsinooma)
Seksuaalisuus
- Ota puheeksi, tarvittaessa seksuaalineuvojan tai -terapeutin vastaanotto
Hormonitoiminta
- Ota puheeksi erityisesti kun
- hoidot tulevat aiheuttamaan menopaussin pre- tai perimenopausaalisella
- hormonikorvaushoito joudutaan keskeyttämään syövän hoidon takia
- Mahdollinen hormonikorvaushoito
- Muiden oireiden hormoniton hoito
- Vasomotoriset oireet
- SSRI ja SNRI, fetsolinetantti
- Unettomuus
- Lääkkeettömät hoidot, liikunta, melatoniini, doksepiini, mirtatsapiini (kts. Unettomuuden käypä hoito -suositus)
- Lisääntynyt kardiovaskulaarisairauksien riski (erityisesti jos ylipainoa, olemassa oleva verenpainetauti tai hyperkolesterolemia)
- Ohjaa työterveys- tai perusterveydenhuoltoon
- Vasomotoriset oireet
Lymfaturvotus
- Huomioi suuren riskin potilailla (LND ja sädehoito, LND ja taksaanihoidot) jo hoitoa suunniteltaessa:
- Vartijaimusolmukemenetelmät
- Tukitekstiilit ennalta ehkäisevästi
- Fysioterapeutin neuvonta turvotusta vähentävää liikuntaa varten
- Tarkista status kontrollikäynneillä ja tee tarvittaessa lähete/maksusitoumus painetekstiilejä (sukat, sukkahousut, housuliivit; 2 paria) varten
- Huomioi tukitekstiilien uusiminen vuosittain, kirjaa diagnoosi ja tarve myös sairaskertomukseen seurannan loppuessa!
Neuropatia
- Erityisesti paklitakseli/dosetakseli- tai sisplatiinipohjaista hoitoa saavilla:
- Reagoi nopeasti vaihtamalla sytostaattihoitoa tai annosreduktioin
- Oireiden hoito:
- Duloksetiini (SSRI/SNRI, trisykliset antidepressantit), tramadoli (kts. Kipu Käypä hoito -suositus), kapsaisiinilaastari 179 mg, 1 % mentoligeeli
Fatiikki
- Ota puheeksi, kysy unihäiriöistä, kivusta, mielialasta, lisäravinteiden käytöstä
- Poissulje anemia, hypotyreoosi, sydänsairaudet
- Kannusta fyysiseen aktiivisuuteen, ohjaa tukiryhmiin, psykososiaalisiin interventioihin (mm. kognitiivinen käyttäytymisterapia)
Luukato
- Huomioi suuren riskin potilailla (hoidoilla aiheutettu menopaussi eikä hormonikorvaushoidon mahdollisuutta, hoito aromataasi-inhibiittoreilla):
- D-vitamiini 10-20 mikrog/vrk + kalsiumin saanti ravinnosta ja korvauksella vähintään 800-900 mg /vrk, kts. Osteoporoosin Käypä hoito -suositus
- DXA, erityisesti jos myös vajaaravitsemusta tai pitkäaikaista po kortisonin käyttöä
Työhön paluu
- Kuntoutussuunnitelma / TYÖOTE-malli
- Yhteistyö työterveyshuollon kanssa